��Ŀ����
ʵ�������������;ʮ�ֹ㷺�����������Ʊ����塣
��1��ijС��ͬѧ����4 mol/L����������230 mL 0.4mol/L ������Һ����ȡ��4 mol/L������ ���� ������������mL��ʵ������Ҫ�õ��IJ��������������� ���� �������������� ����Ͳ������ �ձ�����ͷ�ιܡ�
��2������ʵ�����ʹ���Ƶ���ҺŨ��ƫ�͵���������������
���� A������ƿϴ�Ӻ�δ����
���� B����Һʱ����������Һ����
���� C������ʱ����ˮ���������̶��ߣ��ֵ���һЩ
���� D������ʱ�����ӿ̶���
���� E��װ���Լ�ƿʱ����������Һ����
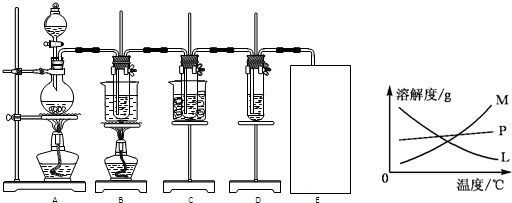
����16�֣���仯ѧ�����ս����̿���Ҫ�ɷ�ΪMnO2����Ũ�����ϼ��ȣ������������ȵõ�����������֪Cl2�ͼ���Һ�ڲ�ͬ�����£��õ��IJ��ﲻͬ��ij��ȤС������ͼ��ʾװ����ȡ����ء��������ƺ�̽����ˮ�����ʡ��� 3Cl2+6KOH����![]() KClO3+5KCl+3H2O ��
KClO3+5KCl+3H2O ��
 |
����
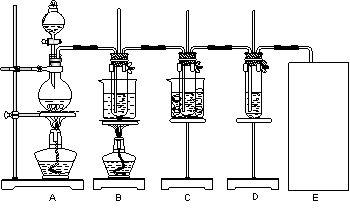
�� ͼ�У�AΪ��������װ�ã�B���Թ���ʢ��15 mL 30% KOH��Һ��������ˮԡ�У�C���Թ���ʢ��15 mL 8% NaOH��Һ�������ڱ�ˮԡ�У�D���Թ��������ɫʯ����Һ��
����д���пհף�
��1����ȡ����ʱ����Բ����ƿ�����һ�������Ķ������̣�ͨ������������ (����������)��Բ����ƿ�м���������Ũ���ᡣװ��A�з�Ӧ�����ӷ���ʽ�������� ��������������������
��2��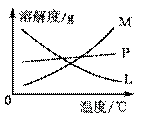 ��Ӧ��Ͼ���ȴ��B���Թ����д���������������ͼ�з��ϸþ����ܽ�����ߵ��������� (������ĸ)����B���Թ��з�����þ���ķ������������� (��ʵ���������)����С��ͬѧ�����Ƶõ�����ز���ƫ�ͣ����ܵ�һ��ԭ����Cl2�к������ʣ������ʳɷ��������� ����ˮ�����⣬�ѧʽ��,��θĽ��������������������������������������������������������������� ��
��Ӧ��Ͼ���ȴ��B���Թ����д���������������ͼ�з��ϸþ����ܽ�����ߵ��������� (������ĸ)����B���Թ��з�����þ���ķ������������� (��ʵ���������)����С��ͬѧ�����Ƶõ�����ز���ƫ�ͣ����ܵ�һ��ԭ����Cl2�к������ʣ������ʳɷ��������� ����ˮ�����⣬�ѧʽ��,��θĽ��������������������������������������������������������������� ��
��3��ʵ���пɹ۲쵽D���Թ�����Һ����ɫ���������±仯������д�±��еĿհף�
| ʵ������ | ԭ�� |
| ��Һ�������ɫ��Ϊ���� ɫ | �� ������ˮ��Ӧ���ɵ�H��ʹʯ���ɫ |
| �����Һ��Ϊ��ɫ | �� ������������������������������������������ |
��4������װ��ͼ�����л���ȱ�ٵ�ʵ��װ�ã���ע���Լ���
��ÿ��2�֣���1��25.0 250mL����ƿ ������ ��2��BC
![]() ��1����Һ©��
��1����Һ©�� ![]()
��2��M��1�֣� ���� ��1�֣�
HCl ��װ��A��B֮���һ��ʢ����ʳ��ˮ��ϴ��ƿ
��3���� ������ˮ��Ӧ���ɵ�HClO����Ư���ԣ�ʹ����Һ��ɫ
��4��
������ÿ��2�֣�

 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�