摘要:23. 负极2 Fe- -2e-= 2Fe2+ 正极
网址:http://m.1010jiajiao.com/timu_id_413790[举报]
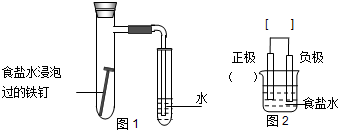
某小组按图1所示的装置探究铁的吸氧腐蚀.
完成下列填空:
(1)图2 是图1所示装置的示意图,在图2的小括号内填写正极材料的化学,在方括号内用箭头表示出电子流动的方向.
(2)写出正、负极反应的方程式.正极:
(3)按图1装置实验,约8分钟才看到的导管中液柱上升,
下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.用食盐水浸泡过的铁钉再蘸取铁粉和炭粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(4)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管.这一措施
(5)有同学观察到图1装置在组装时就会使导管中液面低于试管中液面,导致实验时导管中液柱上升需要更多的时间.图1装置组装时,使导管中液面低于试管中液面的原因是
查看习题详情和答案>>
完成下列填空:
(1)图2 是图1所示装置的示意图,在图2的小括号内填写正极材料的化学,在方括号内用箭头表示出电子流动的方向.
(2)写出正、负极反应的方程式.正极:
2H2O+O2+4e-=4OH-
2H2O+O2+4e-=4OH-
,负极:Fe-2e-=Fe2+
Fe-2e-=Fe2+
.(3)按图1装置实验,约8分钟才看到的导管中液柱上升,
下列措施可以更快更清晰地观察到液柱上升的是
abc
abc
.a.用纯氧气代替具支试管内的空气
b.用食盐水浸泡过的铁钉再蘸取铁粉和炭粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(4)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管.这一措施
不行
不行
(填“可行”或“不行”).(5)有同学观察到图1装置在组装时就会使导管中液面低于试管中液面,导致实验时导管中液柱上升需要更多的时间.图1装置组装时,使导管中液面低于试管中液面的原因是
不论是后塞塞子还是后将导管插入水中,都会造成容器中气体体积减小,压强增大,使导管中液面低于试管中液面
不论是后塞塞子还是后将导管插入水中,都会造成容器中气体体积减小,压强增大,使导管中液面低于试管中液面
.消除这一现象的简单操作是用针筒从橡胶塞处抽气或把橡皮塞换成带分液漏斗的单孔塞
用针筒从橡胶塞处抽气或把橡皮塞换成带分液漏斗的单孔塞
.
回答下列问题
(1)画出磷原子的原子结构示意图: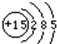
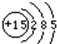 .
.
(2)写出H2S分子的电子式: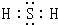
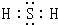 .
.
(3)写出表示含有8个质子,10个中子的原子的化学符号:
(4)已知阴离子aXm-和阳离子bYn+具有相同的核外电子排布,则a、b、m、n之间的关系为a=
(5)用电子式表示氯化镁的形成过程:
 .
.
(6)写出Na2O2中所含化学键的类型
(7)拆开1mol H-H键,1mol N-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ:
则1mol N2完全转化成NH3
(8)利用下列反应:Fe+Cu2+=Fe 2++Cu 制一个化学电池,写出电极反应式:
负极:
查看习题详情和答案>>
(1)画出磷原子的原子结构示意图:
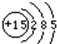
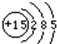
(2)写出H2S分子的电子式:
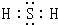
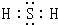
(3)写出表示含有8个质子,10个中子的原子的化学符号:
818O
818O
.(4)已知阴离子aXm-和阳离子bYn+具有相同的核外电子排布,则a、b、m、n之间的关系为a=
b-n-m
b-n-m
.(5)用电子式表示氯化镁的形成过程:


(6)写出Na2O2中所含化学键的类型
离子键,非极性键;
离子键,非极性键;
.(7)拆开1mol H-H键,1mol N-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ:
则1mol N2完全转化成NH3
放出
放出
热量(填“吸收”或“放出”)92
92
kJ;(8)利用下列反应:Fe+Cu2+=Fe 2++Cu 制一个化学电池,写出电极反应式:
负极:
Fe-2e-═Fe2+
Fe-2e-═Fe2+
;正极Cu2++2e-═Cu
Cu2++2e-═Cu
.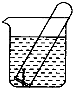 如图所示,水槽中试管内有一枚铁钉,放置数天观察:
如图所示,水槽中试管内有一枚铁钉,放置数天观察:(1)铁钉在逐渐生绣.
(2)若试管内液面上升,发生
吸氧
吸氧
腐蚀,电极反应:负极:Fe-2e-=Fe2+
Fe-2e-=Fe2+
,正极:2H2O+O2+4e-=4OH-
2H2O+O2+4e-=4OH-
(3)若试管内液面下降,则原溶液呈
酸
酸
性,发生的电极反应:负极:Fe-2e-=Fe2+
Fe-2e-=Fe2+
,正极:4H++4e-=2H2↑
4H++4e-=2H2↑
. 为了研究金属腐蚀的原理,某学生做如图实验:先向试管A中加入少量水,将具支试管B的导管末端插入A的水面下:将经过酸洗除锈的铁钉,用蒸馏水洗净后,再用饱和食盐水浸泡一下,投入具支试管B中,并迅速用橡胶塞寒紧试管B.一段时间后,试管A中的导管内液面上升,铁钉表而逐渐产生铁锈.请用电极反应式表示上述过程中电化学腐蚀的反应原理:负极
为了研究金属腐蚀的原理,某学生做如图实验:先向试管A中加入少量水,将具支试管B的导管末端插入A的水面下:将经过酸洗除锈的铁钉,用蒸馏水洗净后,再用饱和食盐水浸泡一下,投入具支试管B中,并迅速用橡胶塞寒紧试管B.一段时间后,试管A中的导管内液面上升,铁钉表而逐渐产生铁锈.请用电极反应式表示上述过程中电化学腐蚀的反应原理:负极Fe-2e-═Fe 2+
Fe-2e-═Fe 2+
,正极O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
. 某课外活动小组同学用如图装置进行实验,试回答下列问题.
某课外活动小组同学用如图装置进行实验,试回答下列问题.(1)若开始时开关K与a连接,则B极的电极反应式为
Fe-2e-=Fe 2+
Fe-2e-=Fe 2+
.有关该实验,下列说法正确的是(填序号)①③
①③
.①A为正极,B为负极
②电子由电极B流出经溶液流向A极
③溶液中Na+向A极移动
④该反应相当于在模拟钢铁的析氢腐蚀
(2)若开关K与b连接,则可模拟工业上离子交换膜法制烧碱,该电池的总反应可表示为(离子方程式)
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
.
| ||
有关该实验,下列说法正确的是(填序号)
②④
②④
.①B为阴极,发生氧化反应
②A极电极反应式可表示为2Cl-=Cl2↑+2e-
③溶液中Na+向A极移动
④若标准状况下B极产生2.24L气体,则电路中通过的电子数为0.2NA.