网址:http://m.1010jiajiao.com/timu_id_412334[举报]
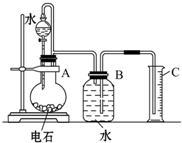 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.(1)烧瓶中发生反应的化学方程式为
(2)分液漏斗与烧瓶间用乳胶管连接的目的是
(3)所用电石质量不能太大,否则
(4)为了得到比较平稳的乙炔气流,实验室通常用
(5)实验中测得排入量筒中水的体积为VL、电石的质量为Wg.则电石中碳化钙的质量分数是
| 0.29V |
| W |
| 0.29V |
| W |
a→e→d→

Ⅱ.同学乙善于利用类比的方法学习,他根据已知资料:硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.提出一个相似的观点:氯气与铁粉反应,当C12足量时生成FeCl3,当铁粉过量时产物是FeCl2.为验证该观点是否正确,他将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分.探究过程如下:
(1)提出假设:A是FeCl3;B是FeCl2.
(2)设计实验方案:分别取A、B的溶液均进行以下实验.请填写下表中的相应空格.
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | 溶液变红色 溶液变红色 |
固体物质中含有FeCl3 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
| ||
| ||
(4)实际应用:FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有FeCl3、FeCl2、CuCl2,同学们设计了从废液中回收Cu的方案:向废液中加入过量的铁粉,充分反应后,过滤.在所得滤渣中加入足量的盐酸,充分反后,再过滤即得到铜.该方案涉及的四种阳离子的氧化性由强到弱的顺序为:
Ⅰ.同学甲选用下图所示仪器制备少量无水FeCl3,仪器连接顺序正确的是a→e→d→ → → → → 。
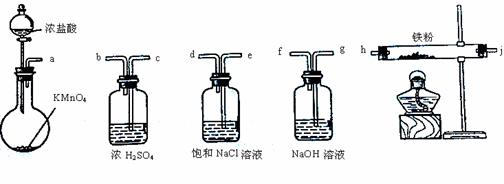
Ⅱ.同学乙善于利用类比的方法学习,他根据已知资料:硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2。提出一个相似的观点:氯气与铁粉反应,当C12足量时生成FeC13,当铁粉过量时产物是FeCl2。为验证该观点是否正确,他将一根细的纯铁丝分别在足量和少量的C12中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分。探究过程如下:
(1)提出假设:A是FeCl3;B是FeCl2。
(2)设计实验方案:分别取A、B的溶液均进行以下实验。请填写下表中的相应空格。
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 |
| 固体物质中含有FeC13 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含 |
(3)根据上述实验结论,写出C12与铁粉加热时发生反应的化学方程式:
_________________________________________________________________;
(4)实际应用:FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有FeC13、FeCl2、CuCl2,同学们设计了从废液中回收Cu的方案:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反后,再过滤即得到铜。该方案涉及的四种阳离子的氧化性由强到弱的顺序为:______________________________;请写出该方案涉及的反应的离子方程式:
______________________________________。
查看习题详情和答案>>
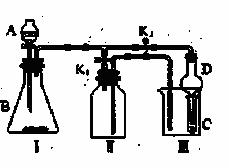
某化学兴趣小组设置了如图所示的实验装置,即可用于制取气体,又可用于验证物质的性质
(1)利用Ⅰ、Ⅱ装置制取气体(K2关闭、K1打开),甲同学认为:利用Ⅱ装置可以收集H2等气体,但不能收集O2 、NO2或NO气体,其理由是 。
(2)乙同学认为:利用Ⅱ装置作简单改进(但不改变瓶口朝向),
也可以收集O2、NO等气体,但不能收集NO2气体,其改进的方法
是 。
(3)丙同学想利用上述装置比较H2SO4、H2CO3和H2SiO3的酸性强弱(不必再选用其它酸性溶液,且通过一次实验就可以达到目的)。实验时,K1关闭、K2打开。锥形瓶内装 固体,装置C(试管)中所盛的试剂是 ;实验确认H2SO4、H2CO3和H2SiO3的酸性强弱出现的现象是
。
(4)丁同学想证明氧化性:Ca(ClO)2 >Cl2 > Br2,实验时,K1关闭、K2打开,则在A中加__________;B中加Ca(ClO)2,C中加________溶液,观察到C中的现象是__________________________;但是此装置在完成这个实验时尚存不足,其不足是_________________________。
I.类比法是化学学习中常用的方法,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是 Fe(NO3)2。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生称FeCl3,当铁粉过量时产物是FeCl2,为了验证该观点是否正确,该同学将一定量的铁粉与Cl2恰好完全反应得到一固体物质,然后通过实验确定其成分。探究过程如下:
⑴提出假设:
假设1:该固体物质是FeCl2
假设2:该固体物质是FeCl3
假设3:该固体物质是
⑵设计实验方案:
取少量固体物质置于烧杯中,加适量水溶解,得到溶液A,然后取两份A溶液分别进行实验,实验现象与结论如下表:
实验方法 | 实验现象 | 结论 |
在溶液中加KSCN溶液 |
| 固体物质中有FeCl3 |
在KMnO4溶液中加少量A 溶液 | KmnO4溶液颜色无明显变化 | 固体物质中不含 |
Ⅱ.电子工业常用30%的FeCl3溶液腐蚀敷在绝缘版上的铜箔,制造印刷电路板。某工程师为了从废液中回收铜,重新获得FeCl3溶液,设计了下列实验步骤:

⑶①写出一个能证明还原性Fe比Cu强的离子方程式: ,该反应在上图步骤 中发生。
②甲、乙、丙、丁四位同学利用上述反应原理,分别设计的原电池如下图所示:


四位同学的设计的原电池装置图,符合上述反应原理的是 。
③请写出正、负极的电解反应式:
正极: 、负极: (电极反应式)。
⑷上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及电极反应式
查看习题详情和答案>>