摘要:下表标出的是元素周期表的一部分元素.回答下列问题:
网址:http://m.1010jiajiao.com/timu_id_403991[举报]
(二)1、 C 2、AD 3、C 4、BC
5、⑴ Ar 、K 、 F 、Br 、M
⑵ H2O HCl PH3 、PH3 ⑶ Cl
6 ⑴ 79 ⑵ 略 ⑶K 、Mg 、Cl 、Se 、C
⑷HClO4、 H2SeO4 、H2CO3 、 Mg(OH)2、 KOH
7 H 、O 、Na 、S 、极性 、共价、 略、NaHSO4+NaHSO3=Na2SO4+H2O+SO2 ↑
8 ⑴Ca 、C 、S 、 ⑵CaC2+2H2O → Ca(OH)2+C2H2↑
⑶CaC2、CS2
9⑴ ⑵> ⑶NH4++H2O
⑵> ⑶NH4++H2O
 NH3?H2O+H+
NH3?H2O+H+
下表标出的是元素周期表的一部分元素,回答下列问题:

(1)表中用字母标出的14种元素中,化学性质最不活泼的是
(2)F,C气态氢化物中其中以
(3)N元素在周期表中的位置是
查看习题详情和答案>>

(1)表中用字母标出的14种元素中,化学性质最不活泼的是
Ar
Ar
(用元素符号表示,下同),非金属性最强的是F
F
,常温下单质为液态的非金属元素是Br
Br
.J、C、F中,原子半径最小的元素是Cl
Cl
;属于过渡元素的是M
M
(该空用字母表示),第六周期的元素共有32
32
种.(2)F,C气态氢化物中其中以
PH3
PH3
(填化学式)最不稳定;第三周期对应的碱性最强的最高价氧化物的水化物的化学式是NaOH
NaOH
,该物质含有的化学键类型是离子键和共价键
离子键和共价键
,用该物质做焰色反应实验,火焰呈黄
黄
色.(3)N元素在周期表中的位置是
第4周期ⅦA族
第4周期ⅦA族
,写出由F单质制取N单质的离子方程式是Cl2+2Br-=2Cl-+Br2
Cl2+2Br-=2Cl-+Br2
.下表标出的是元素周期表的一部分元素,回答下列问题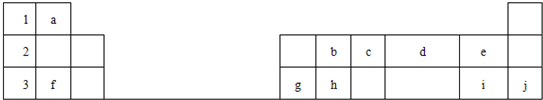
(1)表中列出的10种元素中,化学性质最不活泼的是
(2)分子bd2的电子式
 ,元素e的负一价阴离子的结构示意图
,元素e的负一价阴离子的结构示意图
 .
.
(3)物质bd2和hd2在物理性质上有着巨大差异,其原因是物质bd2属于
(4)元素e的气态氢化物比元素i的气态氢化物
(5)元素f、g的最高价氧化物对应水化物之间反应的离子方程式是
(6)物质fda含有的化学键类型是
查看习题详情和答案>>

(1)表中列出的10种元素中,化学性质最不活泼的是
氩
氩
(填元素名称,下同),非金属性最强的是氟
氟
,原子半径最小的是氢
氢
.(2)分子bd2的电子式




(3)物质bd2和hd2在物理性质上有着巨大差异,其原因是物质bd2属于
分子
分子
晶体,物质hd2属于原子
原子
晶体.(4)元素e的气态氢化物比元素i的气态氢化物
稳定
稳定
(填“稳定”或“不稳定”)(5)元素f、g的最高价氧化物对应水化物之间反应的离子方程式是
Al(OH)3+OH-=[Al(OH)4]-
Al(OH)3+OH-=[Al(OH)4]-
;(6)物质fda含有的化学键类型是
离子键和共价键
离子键和共价键
.下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的15种元素中,化学性质最不活泼的是
(2)B,F,C气态氢化物的化学式分别为
(3)第三周期中原子半径最小的是
查看习题详情和答案>>
| 1 | ||||||||||||||||||
| 2 | D | B | A | |||||||||||||||
| 3 | J | I | H | C | G | F | E | |||||||||||
| 4 | L | K | N | |||||||||||||||
| 5 | M | |||||||||||||||||
| 6 |
Ar
Ar
(用元素符号表示,下同),金属性最强的是K
K
,非金属性最强的是F
F
,常温下单质为液态的非金属元素是Br
Br
,(2)B,F,C气态氢化物的化学式分别为
H2O、PH3、HCl、
H2O、PH3、HCl、
,其中以PH3
PH3
最不稳定.(3)第三周期中原子半径最小的是
Cl
Cl
.