摘要: A.B.C.D四种短周期元素的原子半径依次减小.A与C的核电荷数之比为3:4.D能分别与A.B.C形成电子总数相等的分子X.Y.Z.下列叙述正确的是 A.X.Y.Z的稳定性逐渐减弱B.A.B.C.D只能形成5种单质C.X.Y.Z三种化合物的熔沸点逐渐升高D.自然界存在多种由A.B.C.D四种元素组成的化合物思维方法: .展望高考:[课堂练习]绿色通道[课外作业]绿色通道 第十四课时 非极性分子和极性分子[考纲要求]
网址:http://m.1010jiajiao.com/timu_id_398881[举报]
(05年江苏卷)A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述正确的是 ( )
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只形成5种单质
C.X、Y、Z三种化合物的熔沸点逐渐升高
D.自然界中存在多种由A、B、C、D四种元素组成的化合物
查看习题详情和答案>>[化学选修-物质结构与性质]
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素的原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
根据以上信息,回答下列问题:
(1)上述A、B、C、D四种元素中第一电离能最小的是 ,电负性最大的是 .(填相关元素的元素符号)
(2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 .
(3)A和E可组成离子化合物,其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示:
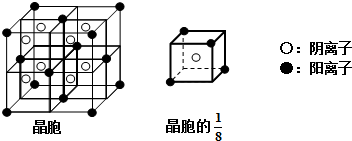
阳离子位于该正方体的顶点或面心;阴离子均位于小正方体中心.该化合物化学式为 .
查看习题详情和答案>>
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素的原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
| … | A | |||||
| B | C | D |
(1)上述A、B、C、D四种元素中第一电离能最小的是
(2)A和D的氢化物中,沸点较高的是
(3)A和E可组成离子化合物,其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示:

阳离子位于该正方体的顶点或面心;阴离子均位于小正方体中心.该化合物化学式为
A、B、C、D四种原子序数依次增大的元素,分布在三个不同的短周期,其中B与C为同一周期的相邻元素,A与D为同一主族.C的单质是燃料电池的一种原料,D是所在周期原子半径最大的元素.下列说法正确的是( )
查看习题详情和答案>>
A、B、C、D、E为前20号元素,原子序数依次增大,其中A、D同主族,B、C、D同周期,B、C、D最高价氧化物对应的水化物均能相互反应生成盐和水.A、B、E的单质均能和水剧烈反应,E+与D的阴离子具有相同的电子层结构.
(1)A、B、C、D四种元素的原子半径由小到大的顺序是 (用元素符号表示).
(2)A和D的氢化物中 (用化学式表示)的沸点较高,原因是 .
(3)写出E单质与水反应的离子方程式 .
(4)B和D形成的晶体中,每个阳离子与它最近且等距的阳离子共有 个.
查看习题详情和答案>>
(1)A、B、C、D四种元素的原子半径由小到大的顺序是
(2)A和D的氢化物中
(3)写出E单质与水反应的离子方程式
(4)B和D形成的晶体中,每个阳离子与它最近且等距的阳离子共有
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:CO(g)+2H2(g)
CH3OH (g)△H1 (反应Ⅰ)该反应的原料CO和H2本身都可作为燃料提供动力,已知这两种物质燃烧的热化学方程式为:
CO(g)+
O2(g)=CO2(g)△H2=-283kJ?mol-1 (反应Ⅱ)
H2(g)+
O2(g)=H2O(g)△H3=-242kJ?mol-1 (反应Ⅲ)
某些化学键的键能数据如下表:
CO的结构为C≡O,请回答下列问题:
(1)反应Ⅰ的焓变△H1=
(2)CH3OH (g)燃烧生成CO2(g)和H2O(g)的热化学方程式为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(g)△H4该反应的焓变△H4=
(3)甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+
O2(g)=CO2(g)+2H2O(l).其工作原理示意图如下:

①在图的横线上标出a、b、c、d四个出入口通入或排出的物质名称(或化学式)
②负极的电极反应式为
查看习题详情和答案>>
| 常温 |
CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
某些化学键的键能数据如下表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
(1)反应Ⅰ的焓变△H1=
-116 kJ?mol-1
-116 kJ?mol-1
.(2)CH3OH (g)燃烧生成CO2(g)和H2O(g)的热化学方程式为:CH3OH(g)+
| 3 |
| 2 |
-651 kJ?mol-1
-651 kJ?mol-1
.(3)甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+
| 3 |
| 2 |

①在图的横线上标出a、b、c、d四个出入口通入或排出的物质名称(或化学式)
②负极的电极反应式为
CH3OH(l)+H2O(l)-6e-=CO2(g)+6H+
CH3OH(l)+H2O(l)-6e-=CO2(g)+6H+
.