摘要:Pb+PbO2+2H2SO42PbSO4+2H2O据此判断下列叙述中正确的是 A.放电时铅蓄电池负极的电极反应为:PbO2+4H++SO42-十2e=PbSO4+2H2OB.充电时铅蓄电池阴极的电极反应为,PbSO4+2e=Pb+SO42-
网址:http://m.1010jiajiao.com/timu_id_393195[举报]
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4 2PbSO4+2H2O,据此判断下列叙述正确的是
2PbSO4+2H2O,据此判断下列叙述正确的是
 2PbSO4+2H2O,据此判断下列叙述正确的是
2PbSO4+2H2O,据此判断下列叙述正确的是 [ ]
A.放电时,H2SO4浓度增加
B.放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4
C.在充电时,电池中每转移1mol电子,理论上生成1mol硫酸
D.在充电时,阴极发生的反应是PbSO4-2e-+2H2O=PbO2+SO42-+4H+
查看习题详情和答案>>
B.放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4
C.在充电时,电池中每转移1mol电子,理论上生成1mol硫酸
D.在充电时,阴极发生的反应是PbSO4-2e-+2H2O=PbO2+SO42-+4H+
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4 2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
2PbSO4+2H2O,根据此反应判断下列叙述中正确的是

A.放电时,H2SO4 浓度降低
B.充电时,电源正极与蓄电池的“—”极连接
C.负极的电极反应式为:Pb+SO42--2e-=PbSO4
D.因PbSO4难溶,铅蓄电池报废后无需回收处理
查看习题详情和答案>>
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4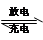 2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
2PbSO4+2H2O,根据此反应判断下列叙述中正确的是

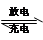 2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.放电时,H2SO4浓度降低 |
| B.充电时,电源正极与蓄电池的“—”极连接 |
| C.负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| D.因PbSO4难溶,铅蓄电池报废后无需回收处理 |
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4 2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.放电时,H2SO4浓度降低 |
| B.充电时,电源正极与蓄电池的“—”极连接 |
| C.负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| D.因PbSO4难溶,铅蓄电池报废后无需回收处理 |
| |||||||||||||||