网址:http://m.1010jiajiao.com/timu_id_383727[举报]
一、选择题(本题包括
1.D 2.C 3.C 4.D 5.C 6.C 7.D 8.D 9.C l0.C
l1.B 12.C 13.C 14.C 15.D 16.C l 7.B l 8.D 19.B 20.A
二、本题包括1小题,共12分。
21.(12分)
(1)B中装无水硫酸铜,检验水蒸气;C中装澄清的石灰水,检验二氧化碳;(每空1分)
(2)验纯后点燃E处的气体,火焰呈蓝色。(2分,不答“验纯”扣1分)
(3)点燃前应验纯;CO有毒,实验要通风;加热时要均匀受热等。(2分)
(4)挥发出来的草酸蒸气与石灰水反应生成了草酸钙沉淀,会干扰CO2的检验(2分)
在装置B和C装置间增加一个装有水(或烧碱溶液)的洗气装置(2分)
三、本题包括3小题,共38分。
22.(每空2分,共12分)
(2)>
(3)A1 +3NH3?H2O=Al(OH)3↓ +3NH
+3NH3?H2O=Al(OH)3↓ +3NH
(4)NH4Al(SO4)2
(5)336
23.(每空2分,共l 2分)
(1)A:Si B:Mg
(2)抑制氯化镁水解
(3)①Si+2NaOH+H2O=Na2SiO3+2H2↑
③ Mg2Si+4HCl=SiH4↑+2MgCl2
24.(每空2分,共14分)
(1)
(2)O2+2CO2+4e =2CO
=2CO
(3)CO2 负极反应产物
②
③ 560
四、本题包括l小题,共l0分。
25.(1)Fe+H2SO4=FeSO4+H2↑(2分)
FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2?6H2O(2分)
(2)解:设生成(NH4)2Fe(SO4)2?6H2O的物质的量为x mol。由上述方程式知:
H2SO4~FeSO4~(NH4)2Fe(SO4)2?6H2 O
1 mol l mol
15×3×10 mol x
mol
mol x
mol
x=0.045
生成(NH4)2Fe(SO4)2?6H2O的质量为:0.045 mol×
(3)① 5、1、8、1、5、4 H2O(2分)
② 83.33%。(2分)
(10分)过量的铁溶于稀硫酸可得硫酸亚铁。等物质的量的硫酸亚铁与硫酸铵作用,能生成溶解度较小的硫酸亚铁铵晶体[![]() ,浅绿色晶体],该晶体的商品名称为摩尔盐。
,浅绿色晶体],该晶体的商品名称为摩尔盐。
(1)写出上述反应的化学方程式。
(2)若用![]()
![]() 硫酸来制备摩尔盐,计算生成摩尔盐的质量。
硫酸来制备摩尔盐,计算生成摩尔盐的质量。
(3)为了测定某批次莫尔盐的纯度,取该产品![]() 配成
配成![]() 溶液,取出
溶液,取出![]() 用
用![]()
![]() 溶液滴定,消耗
溶液滴定,消耗![]() 溶液
溶液![]() 。
。
①配平下列反应式:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
②试求产品中莫尔盐的质量分数 。
查看习题详情和答案>>①称取过氧化钠固体2.00g;
②把这些过氧化钠固体放入气密性良好的气体发生装置中;
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在110mL处恰好与水槽内液面相平;
④将烧瓶中的液体转移到250mL的容量瓶中,然后加入蒸馏水,定容,使液面恰好与刻度相切;
⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
(1)有500mL、250mL、150mL的量筒备用,应选用量程为
(2)有酸式和碱式两种滴定管备用,该实验应选用
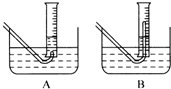
(3)在步骤③测量气体体积时,必须待试管和量筒内的气体都冷却到室温时进行,应选用右图装置中
(4)在步骤⑤中滴定达到终点时,溶液的颜色变化是
(5)该过氧化钠的纯度为
 Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)(1)有500ml、250ml、150ml的量筒备用,应选用量程为
(2)该实验应选用
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面(如图),立即读数会使Na2O2的纯度
(4)在步骤④中用到的仪器除了容量瓶外还需要
(5)在步骤⑤中反应的离子方程式是
(6)该过氧化钠的纯度为
(1)某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸。
①滴定管如图所示,用 滴定管盛装标准浓度的氢氧化钠溶液(填“甲”或“乙”)。

②用滴定的方法来测定盐酸的浓度,实验数据如下所示:
|
实验编号 |
待测HCl溶液的体积(mL) |
滴入NaOH溶液的体积(mL) |
|
1 |
20.00 |
23.00 |
|
2 |
20.00 |
23.10 |
|
3 |
20.00 |
22.90 |
该未知盐酸的浓度为(保留两位有效数字)_______________。
③下列操作会使所测得的盐酸的浓度偏低的是__________:
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数
(2)某课外活动小组为了测定某氯化锶(SrCl2)样品的纯度,设计了如下方案:称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。
请回答下列问题:
①判断滴定达到终点的现象是_______________________________________________。
②考虑Ag+和Fe3+在酸或碱性溶液中的存在形式,在实施滴定的溶液以呈_____(选填“酸性”、“中性”或“碱性”)为宜。
③在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果________(选填“偏高”、“偏低”或“无影响”)。
查看习题详情和答案>>
Na2O2与水的反应实际是Na2O2+2H2O=2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2=2H2O+O2↑。为了测定某过氧化钠固体的纯度,做如下实验:

①称取过氧化钠固体2.00g;
②把这些过氧化钠固体放入气密性良好的气体发生装置中;
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;
④将烧瓶中的液体转移到250mL的容量瓶中,然后加入蒸馏水,定容,使液面恰好与刻度相切
⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.0100mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLMnO4溶液(此时猛全部以Mn2+存在)
(1)有酸式和碱式两种滴定管备用,该实验应选用 ,理由是 。
(2)在步骤③测量气体体积时,必须待试管和量筒内的气体都冷却到室温时进行,应选用上图装置中 。为使量筒为液面恰好与水槽内液面相平,应进行的操作是 。
(3)用酸性KMnO4溶液滴定所配制的溶液,发生反应的离子方程式是 。
(4)在步骤⑤中滴定达到终点时,溶液的颜色变化是 。
(5)该过氧化钠的纯度为 (实验中得到气体体积均看作为标准状况下)。
查看习题详情和答案>>


