摘要:(分)已知某溶液中含有4种离子:A+.B一.H+.OH一.对这4种离子浓度的大小比较.有以下3种说法.请判断离子浓度大小顺序是否正确.你认为正确的请在相应的空格内填上符合这种情况的A+和B+组成物质的化学式(只写一种情况.可以是一种溶质.或两种溶质),你认为一定不正确的.请在相应的空格内填上你选择“不正确 的理由.供选择的离子有:Na+.Ag+.NH4+.Cl-.NO3-.CH3COO-.H+.OH- (1)[B- ]>[A+]>[H+]>[OH- ]: . (2)[A+]>[B- ]>[OH- ]>[H+]: . (3)[H+]>[B- ]>[A+]>[OH- ]: .
网址:http://m.1010jiajiao.com/timu_id_38236[举报]
某溶液x含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.20mol?L-1(不考虑水的电离及离子的水解).为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是( )


| A、无色气体可能是NO和CO2的混合物 | B、由步骤③可知,原溶液肯定存在Fe3+ | C、溶液X中所含离子种类共有4种 | D、另取100mL原溶液x,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的同体质量为2.4g |
已知某FeCl3样品中含有少量FeCl2杂质,某实验小组要测定其中铁元素的质量分数,进行了一系列实验,其操作步骤如图所示:
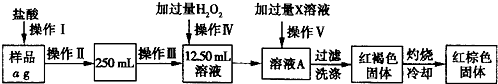
根据如图所示流程示意图,请回答下列问题:
(1)操作Ⅰ中,在溶解样品时,滴加盐酸的作用是
(2)操作Ⅱ中,所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须有
a.50mL烧杯
b.50mL量筒
c.25.00mL滴定管
(3)操作ⅠV中加入过量H2O2,将Fe2+完全氧化为Fe3+,完成并配平该离子方程式:
(4)检验沉淀是否已经洗涤干净的操作步骤是
(5)在最后一步操作中,将沉淀物转移到
(6)若坩埚的质量是W1g,坩埚与加热后固体的总质量是W2g,则样品中铁元素的质量分数是
×100%
×100%(列出原始计算式);若称量准确,最终测量的结果偏大,则造成误差的原因可能是
查看习题详情和答案>>

根据如图所示流程示意图,请回答下列问题:
(1)操作Ⅰ中,在溶解样品时,滴加盐酸的作用是
增强溶液的酸性,抑制Fe3+水解
增强溶液的酸性,抑制Fe3+水解
.(2)操作Ⅱ中,所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须有
250mL容量瓶
250mL容量瓶
(填仪器名称),操作Ⅲ必须用到的仪器是c
c
(填编号).a.50mL烧杯
b.50mL量筒
c.25.00mL滴定管
(3)操作ⅠV中加入过量H2O2,将Fe2+完全氧化为Fe3+,完成并配平该离子方程式:
2
2
Fe2++1
1
H2O2+2
2
H+
H+
=2
2
Fe3++2
2
H2O.(4)检验沉淀是否已经洗涤干净的操作步骤是
取少量最后一次洗出液,滴加硝酸,再滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净
取少量最后一次洗出液,滴加硝酸,再滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净
.(5)在最后一步操作中,将沉淀物转移到
坩埚
坩埚
(填仪器名称)中灼烧、冷却后,用天平称量红棕色固体的质量为m1g,再次重复操作,称量其质量为m2g,若m1-m2=0.3,则接下来还应进行的操作是应再次灼烧、冷却称量,直至两次质量差小于0.1g
应再次灼烧、冷却称量,直至两次质量差小于0.1g
.(6)若坩埚的质量是W1g,坩埚与加热后固体的总质量是W2g,则样品中铁元素的质量分数是
| 14(w2-w1) |
| a |
| 14(w2-w1) |
| a |
固体加热时未充分反应变为Fe2O3
固体加热时未充分反应变为Fe2O3
(写出一种原因即可).已知某无色透明溶液中仅含有包括Na+和CH3COO-在内的四种离子.请回答下列问题.
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
①
(2)用离子方程式表示CH3COONa溶液显碱性的原因:
(3)当该溶液中溶质为两种,且溶液呈碱性时,四种离子的物质的量浓度由大到小的排列顺序可能为(写出两种):①
(4)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是
A.由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.由0.1mol/L的CH3COONa溶液与0.1mol/L的NaOH溶液等体积混合而成
C.由0.1mol/L的CH3COONa溶液与0.1mol/L的CH3COOH溶液等体积混合而成.
查看习题详情和答案>>
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
①
CH3COONa
CH3COONa
;②CH3COONa和CH3COOH
CH3COONa和CH3COOH
; ③CH3COONa和NaOH
CH3COONa和NaOH
.(2)用离子方程式表示CH3COONa溶液显碱性的原因:
CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
 CH3COOH+OH-
CH3COOH+OH-CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
; CH3COOH+OH-
CH3COOH+OH-(3)当该溶液中溶质为两种,且溶液呈碱性时,四种离子的物质的量浓度由大到小的排列顺序可能为(写出两种):①
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
、②c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
;(4)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是
C
C
(填序号).A.由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.由0.1mol/L的CH3COONa溶液与0.1mol/L的NaOH溶液等体积混合而成
C.由0.1mol/L的CH3COONa溶液与0.1mol/L的CH3COOH溶液等体积混合而成.
已知某无色透明溶液中仅含有包括Na+和CH3COO-在内的四种离子.请回答下列问题.
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
①
(2)用离子方程式表示CH3COONa溶液显碱性的原因:
(3)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是
A.由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.由0.1mol/L的CH3COONa溶液与0.1mol/L的NaOH溶液等体积混合而成
C.由0.1mol/L的CH3COONa溶液与0.1mol/L的CH3COOH溶液等体积混合而成
(4)当该溶液中溶质为两种,且溶液呈碱性时,四种离子的物质的量浓度由大到小的排列顺序可能为(写出两种):①
查看习题详情和答案>>
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
①
CH3COONa
CH3COONa
;②CH3COONa和CH3COOH
CH3COONa和CH3COOH
; ③CH3COONa和NaOH
CH3COONa和NaOH
.(2)用离子方程式表示CH3COONa溶液显碱性的原因:
CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
 CH3COOH+OH-
CH3COOH+OH-CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
; CH3COOH+OH-
CH3COOH+OH-(3)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是
C
C
(填序号);A.由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.由0.1mol/L的CH3COONa溶液与0.1mol/L的NaOH溶液等体积混合而成
C.由0.1mol/L的CH3COONa溶液与0.1mol/L的CH3COOH溶液等体积混合而成
(4)当该溶液中溶质为两种,且溶液呈碱性时,四种离子的物质的量浓度由大到小的排列顺序可能为(写出两种):①
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
、②c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
.(14分)已知某无色透明溶液中仅含有包括Na+和CH3COO-在内的四种离子。
请回答下列问题。
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
① ;② ;③ 。
(2)用离子方程式表示CH3COONa溶液显碱性的原因: ;
(3)当该溶液中溶质为两种,且溶液呈碱性时,四种离子的物质的量浓度由大到小的排列顺序可能为(写出两种):① 、② ;
(4)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是 (填序号)。
A.由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.由0.1mol/L的CH3COONa溶液与0.1mol/L的NaOH溶液等体积混合而成
C.由0.1mol/L的CH3COONa溶液与0.1mol/L的CH3COOH溶液等体积混合而成