网址:http://m.1010jiajiao.com/timu_id_343960[举报]
一、选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意。)
1.C 2.B 3.B 4.B 5.D 6.D 7.B 8.A 9.B
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确得2分,但只要选错一个就得0分)
10.C 11.C 12.BC 13.D 14.AC 15.AD 16.AB 17.D 18.BD
三、(本题包括3小题,共32分)
19.(10分)
(1)①-----化学.files/image569.gif) [或
[或-----化学.files/image569.gif) 和
和-----化学.files/image572.gif) ](2分)
](2分)
②将-----化学.files/image574.gif) 晶体在干燥的
晶体在干燥的-----化学.files/image194.gif) 气流中加热(1分)
气流中加热(1分)
②关闭-----化学.files/image579.gif) ,打开
,打开-----化学.files/image581.gif) ,通入足量空气后,再打开
,通入足量空气后,再打开-----化学.files/image579.gif) ,关闭
,关闭-----化学.files/image581.gif) (2分)
(2分)
③D中碱石灰会吸收空气中水蒸气和-----化学.files/image078.gif) 等酸性气体,产生误差,测得
等酸性气体,产生误差,测得-----化学.files/image585.gif) 偏大,
偏大,-----化学.files/image587.gif) 偏小(2分)
偏小(2分)
④-----化学.files/image589.gif) (2分)
(2分)
20.(12分)
(2) -----化学.files/image096.gif) (1分) (3)②③(2分)
(1分) (3)②③(2分)
(5)①-----化学.files/image592.gif) (1分)
(1分)
-----化学.files/image594.gif) (血红色)(1分)
(血红色)(1分)
②-----化学.files/image279.gif) 氧化
氧化-----化学.files/image351.gif) ,使平衡
,使平衡-----化学.files/image598.gif)
-----化学.files/image306.gif)
-----化学.files/image600.gif) 左移,红色消失(2分)
左移,红色消失(2分)
③取一支试管,加入少量-----化学.files/image602.gif) 溶液和几滴
溶液和几滴-----化学.files/image604.gif) 溶液,溶液变为红色,再加入适量
溶液,溶液变为红色,再加入适量-----化学.files/image279.gif) 振荡,产生气泡,红色褪去,说明是
振荡,产生气泡,红色褪去,说明是-----化学.files/image279.gif) 氧化了溶液的
氧化了溶液的-----化学.files/image351.gif) 离子使溶液褪色(2分)
离子使溶液褪色(2分)
说明:(1)加入-----化学.files/image279.gif) 与
与-----化学.files/image604.gif) 溶液的顺序可以互换;(2)上面离子方程式的
溶液的顺序可以互换;(2)上面离子方程式的-----化学.files/image351.gif) 写成
写成-----化学.files/image604.gif) 不扣分;(3)简答中要有仪器、试剂、操作、现象、结论共5个要点,现象“产生气泡”和“红色褪去”2点不能少;(4)若把“溶液褪色”答成“溶液变为黄色或棕色”照样给分。
不扣分;(3)简答中要有仪器、试剂、操作、现象、结论共5个要点,现象“产生气泡”和“红色褪去”2点不能少;(4)若把“溶液褪色”答成“溶液变为黄色或棕色”照样给分。
(6)第六步:还原性(1分) -----化学.files/image096.gif) 在人体血红蛋白中起传送
在人体血红蛋白中起传送-----化学.files/image300.gif) 的作用,
的作用,-----化学.files/image357.gif) 没有此功能,服用
没有此功能,服用-----化学.files/image611.gif) 可防止药品的
可防止药品的-----化学.files/image096.gif) 氧化成
氧化成-----化学.files/image357.gif) (或答成人体只能吸收
(或答成人体只能吸收-----化学.files/image096.gif) ,
,-----化学.files/image096.gif) 在人体血红蛋白中起传送
在人体血红蛋白中起传送-----化学.files/image300.gif) 的作用,服用
的作用,服用-----化学.files/image611.gif) 可防止药品的
可防止药品的-----化学.files/image096.gif) 氧化成
氧化成-----化学.files/image357.gif) )(2分)
)(2分)
21.(10分)
(1) -----化学.files/image046.gif) 、
、-----化学.files/image362.gif) (2)
(2) -----化学.files/image046.gif) 、
、-----化学.files/image364.gif) (3)
(3) -----化学.files/image364.gif) 、
、-----化学.files/image362.gif) (每空1分,全对4分,可以互换)
(每空1分,全对4分,可以互换)
(5) -----化学.files/image368.gif) (1分)
(1分) -----化学.files/image572.gif) (1分)
(1分)
(6) -----化学.files/image618.gif)
-----化学.files/image620.gif) (2分)
(2分)
(7)将沉淀A、F洗涤,小心干燥,分别称量(2分)
四、(本题包括3小题,共37分)
22.(共10分)
(1) -----化学.files/image622.gif) (2分)
(2分)
(2) -----化学.files/image624.gif) 、
、-----化学.files/image078.gif) (2分); 不需要(1分)
(2分); 不需要(1分)
(3)22% (2分)
(4) -----化学.files/image627.gif) (1分); 450(2分)
(1分); 450(2分)
23.(15分) w.w.w.k.s.5.u.c.o.m
(1) -----化学.files/image629.gif) (2分)
(2分)
(2)乙(1分) 流程乙中原料-----化学.files/image423.gif) 来源丰富,价格低,工艺流程简单、技术成熟。(2分)
来源丰富,价格低,工艺流程简单、技术成熟。(2分)
(3)①AD(2分)
②经蒸发、浓缩、冷却至
③-----化学.files/image632.gif) (1分) 取出少许滤液置于试管,加稀盐酸至溶液呈酸性后,过滤得出
(1分) 取出少许滤液置于试管,加稀盐酸至溶液呈酸性后,过滤得出-----化学.files/image042.gif) ,再往滤液中加
,再往滤液中加-----化学.files/image106.gif) 溶液,如有白色沉淀即可证明含有
溶液,如有白色沉淀即可证明含有-----化学.files/image632.gif) (2分)
(2分)
④解:若该反应完全得到-----化学.files/image426.gif) :
:
-----化学.files/image638.gif) (1分)
(1分)
若蒸发浓缩得到的-----化学.files/image440.gif) 溶液为饱和溶液,其所含的
溶液为饱和溶液,其所含的-----化学.files/image426.gif) :
:
-----化学.files/image641.gif) (1分)
(1分)
-----化学.files/image643.gif) ,则该溶液尚未饱和,
,则该溶液尚未饱和,
-----化学.files/image645.jpg) 24.(11分)
24.(11分)
(1) -----化学.files/image647.gif) (2分)
(2分)
(2)0.75(2分)
(3)①c;(1分)②参看右图(2分)
(4) -----化学.files/image649.gif) (2分)
(2分)
(5)B、D(2分)
五、(本题包括1小题,9分) w.w.w.k.s.5.u.c.o.m
25.(9分)
(1)AD(2分)
(2)Ⅰ.甲酸钠;氧化反应,取代反应。(3分)
Ⅱ.反应②:-----化学.files/image651.jpg) (2分)
(2分)
反应⑥:-----化学.files/image653.jpg) (2分)
(2分)
六、选做题(本题包括2小题,每小题10分。考生只能选做一题。26小题为“有机化学基础”内容的试题,27小题为“物质结构与性质”内容的试题)
26.(10分)答:
(1)①液体分为两层,上层液体无色,下层液体仍是红棕色;②溴水褪色,产生白色浑浊;③活泼。(每空1分,共3分)
(2)Ⅰ.-----化学.files/image655.gif) (1分)
(1分)
Ⅱ.-----化学.files/image657.jpg) (2分)
(2分)
(3) Ⅰ.-----化学.files/image659.jpg) (2分)
(2分)
Ⅱ.先将-----化学.files/image498.gif) 保护起来,防止酚羟基被
保护起来,防止酚羟基被-----化学.files/image662.gif) 氧化,通过反应⑥再重新生成酚羟基。(1分)
氧化,通过反应⑥再重新生成酚羟基。(1分)
Ⅲ.-----化学.files/image664.gif) 过量,使化学平衡向正反应方向移动;或边反应边蒸馏降低
过量,使化学平衡向正反应方向移动;或边反应边蒸馏降低-----化学.files/image666.gif) 的浓度,使化学平衡向正反应方向移动。(1分)
的浓度,使化学平衡向正反应方向移动。(1分)
27.(10分)
(1) -----化学.files/image668.gif) (1分)
(1分)
(2) -----化学.files/image235.gif) 分子结构为
分子结构为-----化学.files/image671.gif) ,键能大,难断裂生成氮的化合物
,键能大,难断裂生成氮的化合物
-----化学.files/image076.gif) 分子结构为
分子结构为-----化学.files/image674.gif) ,键能小,易断裂生成氯的化合物 (2分)
,键能小,易断裂生成氯的化合物 (2分)
(3) -----化学.files/image519.gif) 分子中的
分子中的-----化学.files/image006.gif) 原子采取
原子采取-----化学.files/image678.gif) 杂化,
杂化,-----化学.files/image537.gif) 分子中的
分子中的-----化学.files/image006.gif) 原子采取
原子采取-----化学.files/image681.gif) 杂化(2分),D(1分)
杂化(2分),D(1分)
(4)6(1分);①离子晶体的晶格能愈大,晶体熔点愈高 ②晶体中离子电荷数愈大,晶格能愈大,熔点愈高 ③晶体中离子间距离愈小,晶格能愈大,熔点愈高(2分,答对2条即可)
(5) -----化学.files/image683.gif) (1分)
(1分)
下列电极反应正确的是( )
A.钢铁发生电化学腐蚀的正极反应式:Fe-3e-=Fe3+
B.氢氧燃料电池中电解液为硫酸,则正极反应式:O2 + 2H2O + 4e-=OH-
C.氯碱工业电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2 ↑
D.在镀件上电镀锌,用锌作阳极,阳极的电极反应式为:Zn-2e-=Zn2+
查看习题详情和答案>>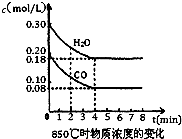 已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.
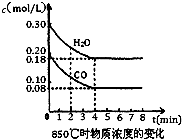
已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.(1)850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O(g),CO和H2O(g)浓度变化如右图所示,下列说法正确的是
A.达到平衡时,反应体系最终会放出49.44kJ热量
B.第4min时,混合气体的平均相对分子质量不再变化,可判断已达到平衡
C.第6min时,若升高温度,反应平衡常数会增大
D.第8min时,若充入CO,会导致v(正)>v(逆),平衡向正反应方向移动
(2)850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO、3.0mol H2O、1.0mol CO2和x mol H2.若要使上述反应开始时向正反应方向进行,则x应满足的条件是
(3)如将H2 与CO2以4:1的体积比混合,在适当的条件下可制得CH4.已知:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ/mol
H2(g)+
| 1 | 2 |
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.负极反应式为
化学反应变化过程及结果的研究。按要求回答问题:
(1)关于反应过程中能量变化的研究:

则:2CO(g)+O2(g)=2CO2(g)△H= kJ·mol-1。
(2)关于反应速率和限度的研究:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3 (g)+ CO2 (g)  CO(NH2)2
(l) + H2O (l),该反应的平衡常数(K)和温度(T / ℃)关系如下:
CO(NH2)2
(l) + H2O (l),该反应的平衡常数(K)和温度(T / ℃)关系如下:
|
T / ℃ |
165 |
175 |
185 |
195 |
|
K |
111.9 |
74.1 |
50.6 |
34.8 |
①焓变ΔH _______0 (填“>”、“<”或“=”)。
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) ,下图(1)是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
,下图(1)是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。

③上图中的B点处,NH3的平衡转化率为 。
(3)关于电化学的研究:
铝是日常生活中用途最多的金属元素,下图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝电极反应式为 。用该电池电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如下图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。


(4)关于电离平衡的研究:
人体血液里存在重要的酸碱平衡: ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
|
c(HCO3-) ∶c(H2CO3) |
1.0 |
17.8 |
20.0 |
22.4 |
|
pH |
6.10 |
7.35 |
7.40 |
7.45 |
试回答:
正常人体血液中,HCO3-的水解程度 电离程度(填“大于”、“小于”、“等于”);
②人体血液酸中毒时,可注射缓解 (填选项);
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③ pH=7.00的血液中,c(H2CO3) c(HCO3-) (填“<”、“>”、“=”)
查看习题详情和答案>>
化学反应变化过程及结果的研究。按要求回答问题:
(1)关于反应过程中能量变化的研究:
则:2CO(g)+O2(g)=2CO2(g)△H= kJ·mol-1。
(2)关于反应速率和限度的研究:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l),该反应的平衡常数(K)和温度(T / ℃)关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数(K)和温度(T / ℃)关系如下:
| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①焓变ΔH _______0 (填“>”、“<”或“=”)。
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
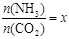 ,下图(1)是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
,下图(1)是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
③上图中的B点处,NH3的平衡转化率为 。
(3)关于电化学的研究:
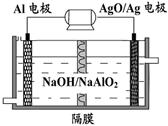
铝是日常生活中用途最多的金属元素,下图为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝电极反应式为 。用该电池电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如下图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。

(4)关于电离平衡的研究:
人体血液里存在重要的酸碱平衡:
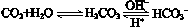 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:| c(HCO3-)∶c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
试回答:
正常人体血液中,HCO3-的水解程度 电离程度(填“大于”、“小于”、“等于”);
②人体血液酸中毒时,可注射缓解 (填选项);
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③ pH=7.00的血液中,c(H2CO3) c(HCO3-) (填“<”、“>”、“=”) 查看习题详情和答案>>
(1)850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O(g),CO和H2O(g)浓度变化如右图所示,下列说法正确的是______(填序号).
A.达到平衡时,反应体系最终会放出49.44kJ热量
B.第4min时,混合气体的平均相对分子质量不再变化,可判断已达到平衡
C.第6min时,若升高温度,反应平衡常数会增大
D.第8min时,若充入CO,会导致v(正)>v(逆),平衡向正反应方向移动
(2)850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO、3.0mol H2O、1.0mol CO2和x mol H2.若要使上述反应开始时向正反应方向进行,则x应满足的条件是______.
(3)如将H2 与CO2以4:1的体积比混合,在适当的条件下可制得CH4.已知:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ/mol
H2(g)+
| 1 |
| 2 |
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是______.
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.负极反应式为______,正极反应式为______.为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定.为此电池工作时必须有部分A物质参加循环,则A物质的化学式是______.实验过程中,若通入了标准状况下空气448L(假设空气中O2体积分数为20%),则熔融盐燃料电池消耗标准状况下CH4______L.
-----化学.files/image577.jpg)