网址:http://m.1010jiajiao.com/timu_id_320452[举报]
某同学为测定某烧碱样品中含NaOH的纯度(设样品中杂质为NaCl),进行如下实验:
(1)称取样品:调节托盘天平到零点后,在天平两盘放质量大小相同纸片,使天平保持平衡,向左盘放一个5g砝码,将游码拨0.2g处;向右盘纸片上缓缓小心加烧碱颗粒到天平达平衡。该操作的错误之处有: 。按如上操作,该同学称取烧碱样品的实际量应是 。
(2)配制溶液:将纸片上的烧碱样品小心移入100mL容量瓶中,加蒸馏水到刻度,盖紧瓶塞,反复倒置摇匀,该操作的错误是 。按此方法所配制得的溶液浓度应 (从“偏高”或“偏低”等词中选填)
(3)取液:将用蒸馏水洗净的锥形瓶再用所配制碱液润洗2~3次,再用蒸馏水洗净的移液管取10mL所配碱液移入锥形瓶,再向瓶中加入约15mL蒸馏水将碱液稀释。此操作中错误之处是 。
(4)滴定:向锥形瓶中加入约2mL酚酞溶液,用浓度为0.5mol?L-1的盐酸标准液进行滴定,滴定时左手操作滴定管,右手猛力振荡锥形瓶,当锥形瓶中溶液颜色刚变粉红色时,停止滴定,记下耗酸体积数,此步操作中错误之处是 。
将(3)(4)操作重复一次
(5)计算:取两次操作耗标准酸液体积平均值为20.00mL,依此数据计算出烧碱样品中含NaOH的质量分数为 。
查看习题详情和答案>>实验室用浓硫酸和乙醇制取乙烯时,常会看到烧瓶中液体变黑,并在制得的乙烯中混有CO2、SO2等杂质。某课外小组设计了如下装置,证明乙烯中混有CO2、SO2,并回答下列问题:

(1)装置A是乙烯的发生装置,图中一处明显的错误是__________________,将反应后的混合气体通入到溴水当中,可能发生的化学反应方程式是:
、 ;
(2)若要检验装置A中所得气体含有SO2,可将混合气体直接通入_______(填代号,下同)装置;若要检验A中所得气体含有CH2=CH2,可将混合气体先通入_____装置,然后通入D装置;
(3)该小组将从装置A出来的混合气体依次通过B、E、D、E,发现通入D之前的石灰水中无明显变化,通入D之后的石灰水变浑浊。请对出现该现象的原因进行合理猜想______________________________________________;
(4)若要将三种气体全部检验出来,且要求所用的试剂瓶最少,则气体从A出来依次通过的装置先后顺序是(假设试剂足量)_______________________。
查看习题详情和答案>>A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素的原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物ACD3与其氢化物CA3反应生成一种盐X,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。
请回答下列问题:
(1)由A、B、D、E四种元素组成的某无机化合物Y受热易分解。写出少量Y溶液与足量Ba(OH)2溶液反应的离子方程式 。
(2)将铝片和镁片用导线连接,插入由A、D、E三种元素组成的稀溶液中构成原电池,则负极的电极反应式为 。
(3)常温下,ACD3的稀溶液与CA3的水溶液混合,可能出现的结果是 。
①pH<7,c(H+)>c(CD![]() )> c(OH-)> c(CA
)> c(OH-)> c(CA![]() )
)
②pH<7,c(CD![]() ) >c(OH-)=c(H+)> c(CA
) >c(OH-)=c(H+)> c(CA![]() )
)
③①pH>7,c(CA![]() )> c(OH-) >c(CD
)> c(OH-) >c(CD![]() )>c(H+)
)>c(H+)
④①pH<=7,c(CA![]() )>c(CD
)>c(CD![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
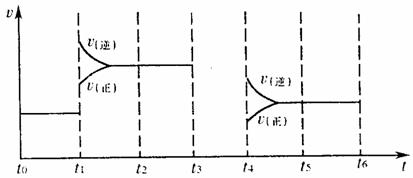
(4)对可逆反应3A2(g)+C2(g) ![]() 2CA3(g),当反应达到平衡时,不断改变条件(不改变A2、C2、CA3的量),下图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是 。
2CA3(g),当反应达到平衡时,不断改变条件(不改变A2、C2、CA3的量),下图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是 。
(5)温度为T℃时,将4amolA2和2amolC2放入1L密闭容器中,充分反应后测得C2的转化率为50%,则该反应的平衡常数为 。
查看习题详情和答案>>| 元素 | 性质或结构信息 |
| X | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼. |
| Y | 二价阳离子的外围电子层排布为3d9 |
| T | 原子核外s轨道电子总数等于p轨道电子总数;人体内含量最多的元素,且其单质是常见的助燃剂 |
| Q | 第三周期主族元素中原子半径最小 |
(1)写出 X3-的一种等电子体的化学式
(2)写出T元素基态原子的核外电子排布图


(3)元素 X、T 的电负性相比,
(4)甲醛(CH2O)分子中σ 键与π 键的个数之比为

(5)Y元素在周期表中位于
(6)在Y的硫酸盐溶液中通入X的气态氢化物至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液.此蓝色沉淀溶解的离子方程式为:
(7)元素X与Q可形成化合物XQ3,根据价层电子对互斥理论判断XQ3的空间构型为:
 (2009?静安区二模)一种兴奋剂X的结构如图所示.下列说法的错误是( )
(2009?静安区二模)一种兴奋剂X的结构如图所示.下列说法的错误是( )