摘要:请回答: (1)写出反应①的化学方程式 ,已知B的燃烧热是1300kJ?mol-1.写出反应②的热化学方程式 . (2)G和H的混合物俗称 .在空气中易失效需密封保存.其原因表示 . (3)E和NO2在室温下可以化合生成一种新的气态化合物.实验测知:取E和NO2混合气体5L.当E所占体积分数分别为20%.60%.反应后气体的体积均为4L(所有气体体积在相同条件下测得).生成的气态化合物的分子式 .反应的化学方程式 .
网址:http://m.1010jiajiao.com/timu_id_290072[举报]
中学常见反应的化学方程式有A+B→X+Y+H2O或H2O+ A+B→X+Y(未配平,反应条件略去),下列问题所涉及反应式中的H2O已经略去。请回答:
(1)常温下,若A为黄绿色气体,B为非金属氧化物,A、B均能使品红溶液褪色,A+B→X+Y,且相对分子质量X>Y,则该反应的化学方程式为________________,检验Y中阴离子的试剂是________________。
(2)若Y是黄绿色气体,且A、B的物质的量之比为1∶4,该反应的化学方程式是 。
(3)若A为常见的金属单质,Y为气态单质,B溶液呈强酸性或强碱性时,A和B反应都能进行。写出A与B反应的离子方程式:_________________;_________________。
(4)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,其中A、B的物质的量之比为1∶4,则反应中氧化剂与还原剂的物质的量之比是 。
(5)若A、B均为化合物,Y为白色沉淀(不含金属元素),B为引起温室效应的主要气体,将B通入某溶液后可生成Y,写出Y可能的化学式______________。写出生成Y的一个离子方程式______________________________。
 请回答有关下列五种气体:H2、O2、NO、NH3、NO2的问题.
请回答有关下列五种气体:H2、O2、NO、NH3、NO2的问题.(1)气体的制备与收集:
①与制取O2 的发生装置相同的是
NH3
NH3
(填化学式,下同),只适合用排水法或排空气法一种方法收集的是NO、NH3、NO2
NO、NH3、NO2
;②以上气体制备反应中,有一反应在原理上与其它反应都不能归为同一类型,请写出实验室制取该气体的方程式
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(2)用右图装置进行喷泉实验(图中夹持装置均已略去).
①若用图1装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发水上喷的操作是
打开止水夹,挤出胶头滴管中的水
打开止水夹,挤出胶头滴管中的水
,该实验的原理是氨气极易溶解于水,致使烧瓶内气体压强迅速减小
氨气极易溶解于水,致使烧瓶内气体压强迅速减小
;②若用图2的装置,请举一例说明引发喷泉的方法:
打开夹子,用手(或热毛巾等)将烧瓶捂热
打开夹子,用手(或热毛巾等)将烧瓶捂热
.(3)若用同一烧瓶分别充满如下气体:①HCl ②NH3 ③NO2进行喷泉实验,实验后烧瓶内溶液液面的高度关系为
①=②>③
①=②>③
(用序号和“>,<或=”表示,下同),所得溶液物质的量浓度大小关系为①=②=③
①=②=③
. 写出木炭与浓硫酸反应的化学方程式
写出木炭与浓硫酸反应的化学方程式C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.
| ||
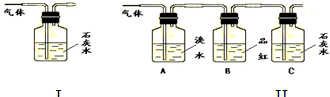
为了验证产物中的二氧化碳气体,甲、乙两同学分别设计如下实验(已知Br2+2H2O+SO2═H2SO4+2HBr):
请回答下列问题
(1)根据Ⅰ装置中石灰水变浑浊的现象能否说明产物中一定有二氧化碳气体?
不能
不能
,理由是因为SO2与石灰水反应生成CaCO3也难溶于水
因为SO2与石灰水反应生成CaCO3也难溶于水
.(2)Ⅱ装置中A的作用是
除去SO2
除去SO2
;B的作用是检验SO2是否已除净
检验SO2是否已除净
.(3)根据B中品红
B中品红不褪色
B中品红不褪色
,C中产生C中产生浑浊(或白色沉淀)
C中产生浑浊(或白色沉淀)
,说明产物中一定有二氧化碳气体.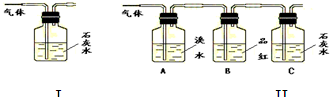 写出木炭与浓硫酸反应的化学方程式______.
写出木炭与浓硫酸反应的化学方程式______.