摘要:为顺式结构. 为反式结构(a.b为不同的原子或原子团).
网址:http://m.1010jiajiao.com/timu_id_287718[举报]
A、B、C、D是中学化学常见的四种短周期元素,已知:
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为
 ,Y与水反应产物的化学式为
,Y与水反应产物的化学式为
查看习题详情和答案>>
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
HClO4>HNO3>H2CO3
HClO4>HNO3>H2CO3
,D元素在元素周期表中的位置是第三周期ⅣA族
第三周期ⅣA族
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
,现有19.2g 铜粉溶解,产生标准状况下气体的体积是4.48
4.48
L.(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
3SiCl4+4NH3═Si3N4+12HCl
3SiCl4+4NH3═Si3N4+12HCl
.(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为


NH3和HClO
NH3和HClO
.A、B、C、D、E、F六种短周期元素,其原子序数依次增大,在所有元素中A的原子半径最小,B原子最外层电子数是次外层的2倍.A、E同主族,D、F同主族,且D、F的原子序数之和为A、E的原子序数之和的2倍,请回答下列问题:
(1)写出下列元素的名称:C
(2)A、C能形成多种化合物,其中C2A4的结构式为
 (用元素符号回答,下同);
(用元素符号回答,下同);
(3)化合物E2D2中存在的化学键类型为
(4)由A、D、E、F四种元素形成的两种化合物,在水溶液中两者反应的离子方程式为
(5)B的单质可与A、D、F形成化合物的浓溶液反应,为检验所有生成物,被检验物质的顺序依次为
查看习题详情和答案>>
(1)写出下列元素的名称:C
氮
氮
;E钠
钠
;(2)A、C能形成多种化合物,其中C2A4的结构式为


(3)化合物E2D2中存在的化学键类型为
离子键、非极性键
离子键、非极性键
;(4)由A、D、E、F四种元素形成的两种化合物,在水溶液中两者反应的离子方程式为
H++HSO3-═H2O+SO2↑
H++HSO3-═H2O+SO2↑
;(5)B的单质可与A、D、F形成化合物的浓溶液反应,为检验所有生成物,被检验物质的顺序依次为
H2O、SO2、CO2
H2O、SO2、CO2
.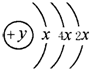 A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空:(1)A元素气态氢化物的电子式
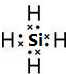
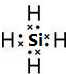
Mg>Si>P>N
Mg>Si>P>N
.(填元素符号)(2)A的最高价氧化物与氢氧化钠反应的离子方程式为
SiO2+2OH-=SiO32-+H2O
SiO2+2OH-=SiO32-+H2O
.(3)A,C,D的最高价氧化物对应水化物的酸性强弱
HNO3>H2SiO3>H3PO4
HNO3>H2SiO3>H3PO4
C的氢化物比D的氢化物沸点高
高
(填“高”或“低”),原因是NH3分子之间存在氢键,故其沸点比PH3的沸点高
NH3分子之间存在氢键,故其沸点比PH3的沸点高
.A、B、C、D、E均为短周期元素,且原子序数逐渐增大.A、D最外层电子数相等且能形成离子化合物,A与B的质子数之和等于C的质子数,A+与 C2-的核外电子数之和等于D+离子的核外电子数,B 原子与 D+离子的核外电子数之和等于 E 原子的核外电子数.
(1)B的元素符号为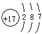
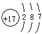 ;由A、C、E三种元素组成的化合物具有漂白性,其电子式为
;由A、C、E三种元素组成的化合物具有漂白性,其电子式为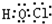
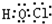 .
.
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
查看习题详情和答案>>
(1)B的元素符号为
N
N
,E的原子结构示意图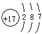
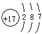
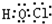
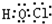
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
.(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
NH4NO3
NH4NO3
,物质乙抑制水的电离HNO3
HNO3
;室温下,若两溶液的pH都为4,则两溶液中水电离的氢离子浓度比为:甲:乙=106
106
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
>
>
7(填“>”“<”“=”),溶液中离子浓度由大到小的顺序为C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C(NH4+)>C(Cl-)>C(OH-)>C(H+)
.(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
H2+2e-+2OH-=2H2O
H2+2e-+2OH-=2H2O
.A、B、C、D、E、F属于短周期主族元素.A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零,C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差.
(1)离子B-的结构示意图为
 ;化合物CE2的分子属于
;化合物CE2的分子属于
 .
.
(2)A、E、F形成的简单离子的半径由大到小的顺序为
(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W?8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一.有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3.该电池的负极反应式为
查看习题详情和答案>>
(1)离子B-的结构示意图为


非极性
非极性
分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程

(2)A、E、F形成的简单离子的半径由大到小的顺序为
S2->O2->Na+
S2->O2->Na+
(用离子符号表示);元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)金刚石(石墨)>晶体硅>氧气
金刚石(石墨)>晶体硅>氧气
.(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W?8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
.(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一.有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3.该电池的负极反应式为
C4H10+13O2--26e-=4CO2+5H2O
C4H10+13O2--26e-=4CO2+5H2O
,电池工作时,电解质里的CO32-向负
负
极移动.