摘要:单质.化合物.氧化物.酸.碱.盐等概念. 教学难点:对单质.化合物.氧化物.酸.碱.盐等概念的理解. [基础知识的归纳与整理] (组织学生根据自己对物质分类知识的掌握情况进行研讨.尝试给常见物质进行简分类.教师可适当指导.最后由教师小结.并以投影形式给出物质分类的知识结构.在学生研讨过程中应提醒学生注意分类的依据以及概念间的从属关系) (概括出物质分类的知识体系后.教师引导学生思考:能否用其它形式对物质进行分类.诸如画知识树等.借此激发学生学习化学的兴趣.可以让学生偿试一下.也可将其留作课后作业). [关键知识点拔] (以投影形式打出表格.鼓励学生经过讨论比较相关的概念.找出这些概念的异同点及其联系.教师适时点拔.强调理解概念应抓住关键字词和相关概念的内在联系.最后师生共同完成表格内容). (一)纯净物和混合物项目 纯净物 混合物 概念 由同一种物质组成 由两种或两种以上的物质混合而成.彼此间不发生化学反应 区别 ①一种物质②对于由分子构成的物质而言.由一种分子构成③有固定的组成④有固定的性质 ①两种或两种以上物质②由不同种分子构成③没有固定的组成④没有固定的性质 联系 (二)单质和化合物项目 单质 化合物 概念 由同种元素组成的纯净物 由不同种元素组成的纯净物 相同点 均为纯净物 均为纯净物 不同点 ①由一种元素组成②单质的分子由同种原子构成 ①由不同种元素组成②化合物分子由不同种原子构成 联系 (三)氧化物 项目 酸性氧化物 碱性氧化物 概念 凡能跟碱起反应生成盐和水的氧化物 凡能跟酸起反应而生成盐和水的氧化物 组成 大多数是非金属氧化物 都是金属氧化物 性质 ①与水反应生成对应的含氧酸(SiO2除外)②与可溶性碱反应生成盐和水 ①与水反应生成可溶性碱②与酸反应生成盐和水 (四)酸.碱.盐项目 酸 碱 盐 概念 电离时生成的阳 离子全部是氢离 子的化合物 电离时生成的阴离子全部是氢氧根离子的化合物 电离时生成金属离子和酸根离子的化合物 相同点 均为化合物.其水溶液都能导电 不同点 酸=H++酸根离子 碱=金属离子+OH- 盐=金属离子+酸根离子 组成特点 一定含氢元素 一定含氢.氧两种元素 一定含有非金属元素 联系 酸+碱→盐+水 [典型例题讲解]
网址:http://m.1010jiajiao.com/timu_id_21740[举报]
一、1.C 2.D 3.A 4.B 5.D
二、
1. ①⑦ ③ ⑤⑨ ④ ⑥⑧
2.(1)NaOH (2)Al (3)氢气 (4)食盐
3
锌
氢氧化钠
HCl
CaO
Cu2(OH)2CO3
H2SO4
酸
单质
氧化物
碱
盐
酸
4.碱 氧化物
酸、碱、盐都是重要的化合物,请回答下列有关问题.
(1)下列不属于复分解反应发生条件的是
A.有水生成 B.有气体生成
C.有单质生成 D.有难溶物生成
(2)观察图1,请简述闻浓盐酸气味的操作方法(或注意事项).
(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
以上实验的正确操作顺序为
(4)用pH试纸测定所配制溶液的酸碱度,应该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g.计算废水中氯化氢的质量分数.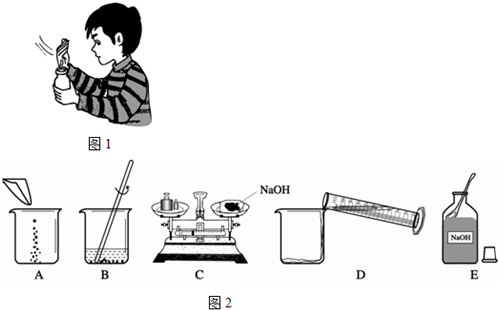
查看习题详情和答案>>
(1)下列不属于复分解反应发生条件的是
C
C
(填字母).A.有水生成 B.有气体生成
C.有单质生成 D.有难溶物生成
(2)观察图1,请简述闻浓盐酸气味的操作方法(或注意事项).
(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
以上实验的正确操作顺序为
ECADB
ECADB
;(用字母代号表示);其中B中的仪器名称是玻璃棒和烧杯
玻璃棒和烧杯
;C操作中出现的错误是砝码和被称量物质放颠倒了
砝码和被称量物质放颠倒了
;若C中砝码的质量为15g,游码的读数为3.5g,则氢氧化钠和纸片的实际总质量为11.5g
11.5g
g.(4)用pH试纸测定所配制溶液的酸碱度,应该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g.计算废水中氯化氢的质量分数.

酸、碱、盐都是重要的化合物,请回答下列有关问题.
(1)下列不属于复分解反应发生条件的是______(填字母).
A.有水生成 B.有气体生成
C.有单质生成 D.有难溶物生成
(2)观察图1,请简述闻浓盐酸气味的操作方法(或注意事项).
(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
以上实验的正确操作顺序为______;(用字母代号表示);其中B中的仪器名称是______;C操作中出现的错误是______;若C中砝码的质量为15g,游码的读数为3.5g,则氢氧化钠和纸片的实际总质量为______g.
(4)用pH试纸测定所配制溶液的酸碱度,应该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g.计算废水中氯化氢的质量分数.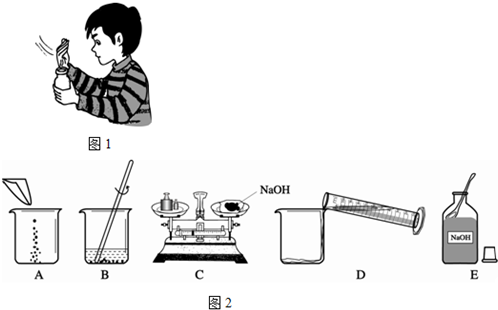
查看习题详情和答案>>
酸、碱、盐都是重要的化合物,请回答下列有关问题.
(1)下列不属于复分解反应发生条件的是______(填字母).
A.有水生成 B.有气体生成
C.有单质生成 D.有难溶物生成
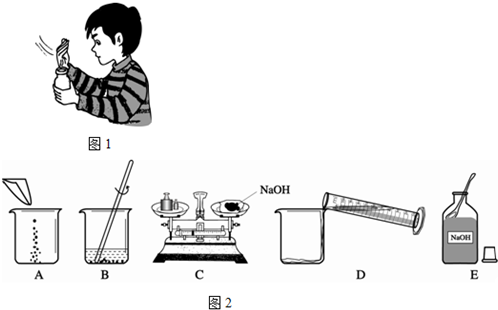
(2)观察图1,请简述闻浓盐酸气味的操作方法(或注意事项).
(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
以上实验的正确操作顺序为______;(用字母代号表示);其中B中的仪器名称是______;C操作中出现的错误是______;若C中砝码的质量为15g,游码的读数为3.5g,则氢氧化钠和纸片的实际总质量为______g.
(4)用pH试纸测定所配制溶液的酸碱度,应该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g.计算废水中氯化氢的质量分数.
查看习题详情和答案>>
(1)下列不属于复分解反应发生条件的是______(填字母).
A.有水生成 B.有气体生成
C.有单质生成 D.有难溶物生成
(2)观察图1,请简述闻浓盐酸气味的操作方法(或注意事项).
(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
以上实验的正确操作顺序为______;(用字母代号表示);其中B中的仪器名称是______;C操作中出现的错误是______;若C中砝码的质量为15g,游码的读数为3.5g,则氢氧化钠和纸片的实际总质量为______g.
(4)用pH试纸测定所配制溶液的酸碱度,应该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g.计算废水中氯化氢的质量分数.

酸、碱、盐都是重要的化合物,请回答下列有关问题。
(1) 下列不属于复分解反应发生条件的是 (填字母)。
下列不属于复分解反应发生条件的是 (填字母)。
| A.有水生成 | B.有气体生成 |
| C.有单质生成 | D.有难溶物生成 |
(2)观察右图,请简述闻浓盐酸气味的操作方法(或注意事项)。

(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
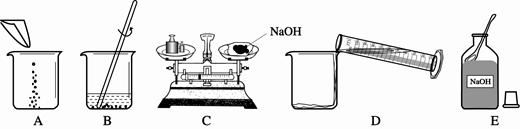
以上实验的正确操作顺序为 ;(用字母代号表示);其中B中的仪器名称是 ;C操作中出现的错误是 ;若C中砝码的质量为15g,游码的读数为3.5 g,则氢氧化钠和纸片的实际总质量为 g。
g,则氢氧化钠和纸片的实际总质量为 g。
(4)用pH试纸测定所配制溶液的酸碱度,应 该如何操作?
该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。计算废水中氯化氢的质量分数。
酸、碱、盐都是重要的化合物,请回答下列有关问题。
(1)下列不属于复分解反应发生条件的是 (填字母)。
| A.有水生成 | B.有气体生成 |
| C.有单质生成 | D.有难溶物生成 |

(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
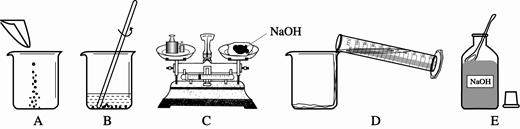
以上实验的正确操作顺序为 ;(用字母代号表示);其中B中的仪器名称是 ;C操作中出现的错误是 ;若C中砝码的质量为15g,游码的读数为3.5g,则氢氧化钠和纸片的实际总质量为 g。
(4)用pH试纸测定所配制溶液的酸碱度,应该如何操作?
(5)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。计算废水中氯化氢的质量分数。 查看习题详情和答案>>