网址:http://m.1010jiajiao.com/timu_id_212252[举报]
 (1)现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;0.96g D的单质跟足量盐酸反应,生成D3+和1.2L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构.
(1)现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;0.96g D的单质跟足量盐酸反应,生成D3+和1.2L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构.①写出元素符号:A
②B、D的最高价氧化物对应水化物相互反应的离子方程式为:
③用电子式表示C与E形成E2C的过程:


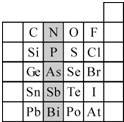
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
①阴影部分元素N在元素周期表中的位置为第
根据元素周期律,预测:酸性强弱 H3AsO4
②元素S的最高正价和最低负价的代数和为
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是
④下列说法正确的是
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.
①写出元素符号:A______,C______,E______.
②B、D的最高价氧化物对应水化物相互反应的离子方程式为:______.
③用电子式表示C与E形成E2C的过程:______.
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
①阴影部分元素N在元素周期表中的位置为第______周期第______族.
根据元素周期律,预测:酸性强弱 H3AsO4______H3PO4.(用“>”或“<”表示)
②元素S的最高正价和最低负价的代数和为______,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度______.(选填“更大”、“更小”或“相同”)
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是______.
④下列说法正确的是______
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.
①写出元素符号:A______,C______,E______.
②B、D的最高价氧化物对应水化物相互反应的离子方程式为:______.
③用电子式表示C与E形成E2C的过程:______.
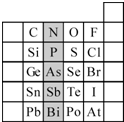
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
①阴影部分元素N在元素周期表中的位置为第______周期第______族.
根据元素周期律,预测:酸性强弱 H3AsO4______H3PO4.(用“>”或“<”表示)
②元素S的最高正价和最低负价的代数和为______,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度______.(选填“更大”、“更小”或“相同”)
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是______.
④下列说法正确的是______
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.
 查看习题详情和答案>>
查看习题详情和答案>>
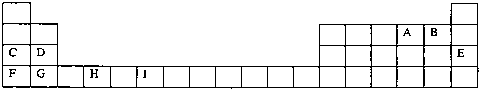
请回答下列问题:
(1)写出元素I的基态原子的价电子排布式
(2)请列举F的金属性比C强的实验事实:
(3)在标准状况下,根据M=
| m | n |
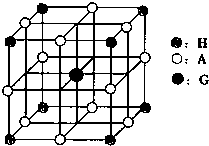
(4)H、A、G三种元素形成的晶体是一种矿物的主要成分,其晶胞结构如图,则该晶体的化学式为
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施。化学反应的焓变一般通过实验进行测定,也可进行理论推算。
(1)实验测得,0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量。写出上述燃烧反应的热化学方程式 。标准状况下11.2L乙硼烷完全燃烧生成液态水时放出的热量是 kJ。
(2)在化学反应过程中,拆开化学键需要吸收能量,形成化学键又会释放能量。已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗496kJ能量,形成水蒸气中的1mol H-O键能够释放463kJ能量。试说明反应2H2(g)+O2(g)=2H2O(g)中的能量变化。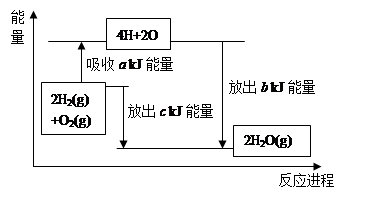
a= ,b= 。又知1mol液态水转化成气态水吸收44 kJ能量,则氢气完全燃烧生成液态水时的热化学方程式为 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。实验中不能直接测出由石墨和氢气生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧热分别如下:
①CH4(g)+2O2(g)=CO2(g)+2H2O ΔH1=-890.3 kJ?mol-1
②C(石墨)+O2(g)= CO2(g) ΔH2= —393.5 kJ?mol-1
③H2(g)+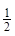 O2(g)=H2O(l) ΔH3= ─285.8 kJ?mol-1
O2(g)=H2O(l) ΔH3= ─285.8 kJ?mol-1
④C(石墨)+2H2(g)= CH4(g) ΔH4
试根据盖斯定律求出石墨生成甲烷的反应热ΔH4= 。