摘要:(1)第三周期8种元素按单质熔点高低的顺序如右图.其中序号“8 代表 ,其中电负性最大的是 .(2)请写出比元素1的原子序数大8的元素的基态原子电子排布式 .(3)元素7的单质晶体中原子的堆积方式如下图甲所示.其晶胞特征如下图乙所示.原子之间相互位置关系的平面图如下图丙所示.
网址:http://m.1010jiajiao.com/timu_id_204617[举报]
已知
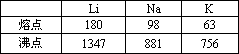
回答问题:(M表示碱金属)(填>或<或=)
(1)ΔH2(Li)________ΔH2(Na),ΔH3(Li)________ΔH3(Na),
(2)已知金属活动性顺序金属锂比钠活泼,则ΔH4(Li)________ΔH4(Na).
(3)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________(填元素符号);其中电负性最大的是________(填图中的序号).

下表是元素周期表的一部分.表中所列字母分别代表一种化学元素.
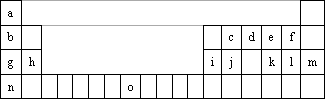
试回答下列问题:
(1)请写出元素O的基态原子电子排布式________.
(2)第三周期8种元素按单质熔点高低的顺序如下图,其中序号“8”代表________(填元素符号);其中电负性最大的是________(填下图中的序号),第一电离能最大的是________(填下图中的序号).
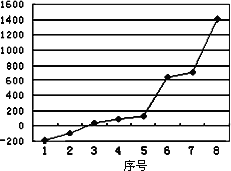
(3)由j原子跟c原子以1∶1相互交替结合而形成的晶体,晶体类型与晶体j相同.两者相比熔点更高的是________(填化学式),试从结构角度加以解释________.
(4)COCl2俗称光气,分子中C原子采取________杂化成键;分子中的共价键含有________(填标号)
a.2个σ键
b.2个π键
c.1个σ键、2个π键
d.3个σ键、1个π键
(4分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| | | | |||||
| | | | a | | | | |
| | b | | c | | | d | |
(1)元素b的基态原子电子排布式为 。
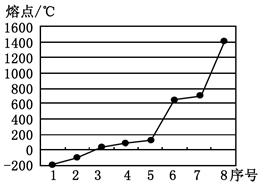
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。 查看习题详情和答案>>
(4分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

(1)元素b的基态原子电子排布式为 。
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
| | | | |||||
| | | | a | | | | |
| | b | | c | | | d | |

(1)元素b的基态原子电子排布式为 。
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
下表是元素周期表的一部分.表中所列的编号分别代表一种化学元素.
试回答下列问题:
(1)请写出⑨代表的元素基态原子电子排布式______.
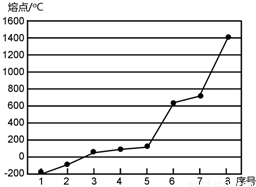
(2)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”代表______(填元素符号);其中电负性最大的是______(填元素符号).
(3)由⑤原子跟②原子以1:1相互交替结合而形成的晶体,其晶型与②对应的一种晶体相同.两者相比熔点更高的是______(填中文名称),原因是:______.
(4)现有含钛的两种颜色的晶体,Ti3+的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为TiCl3?6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 .
.
试推断紫色晶体的化学式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑩ | ⑧ | ⑨ | |||||||||||||||
(1)请写出⑨代表的元素基态原子电子排布式______.
(2)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”代表______(填元素符号);其中电负性最大的是______(填元素符号).
(3)由⑤原子跟②原子以1:1相互交替结合而形成的晶体,其晶型与②对应的一种晶体相同.两者相比熔点更高的是______(填中文名称),原因是:______.
(4)现有含钛的两种颜色的晶体,Ti3+的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为TiCl3?6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
 .
.试推断紫色晶体的化学式为______.
 查看习题详情和答案>>
查看习题详情和答案>>