网址:http://m.1010jiajiao.com/timu_id_199744[举报]
1. C 2. B 3. B 4. B 5. B 6. D 7. B 8. B 9. B 10. C 11. D 12. D 13. B 14. A 15. D 16. B 17. C 18.D 19.A 20. A 21.BC 22.D 23.BD 24.C 25.AD 26.AB 27.B 28.C 29.D 30.D
 31.(3分)(1)
31.(3分)(1)
(2)① CH3―CH=CH―CH=CH―CH3 ② CH2=CH―CH2―CH=CH―CH3(每空1分)
32.(3分)(1)甲醛
(2) C3H6O3 HCOOCH2CH2OH(每空1分)
 (5)
?:
(5)
?: (邻,间等)(1分);?:
(邻,间等)(1分);?: (1分)。
(1分)。
35.(11分)(1)碳碳双键,?CHO (2分)
(2)A、C ; D (2分)
(3)氧化,(1分)
 (2分)
(2分)
 |
|||
 |
(4) ;(2分) (2分)
(1)写出下列反应的化学方程式:
①氯化钡溶液与硫酸钠混合:______________________;
②碳酸钾溶液与稀盐酸混合:______________________;
③氢氧化钡溶液与稀硝酸混合:______________________。
(2)你想过上述复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合。如上述反应①中,实际参加反应的离子是Ba2+和SO42-,而Cl-、Na+则是“旁观者”,并没有参加反应。请你分析上述反应②中实际参加反应的离子是______________;上述反应③中实际参加反应的离子是______________________。
(3)请根据你的想象,在下图右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图。

(1)“盐+酸—→新盐+新酸”是复分解反应中的一种类型。在Na2SiO3溶液中滴入盐酸,生成的新酸是___________(写化学式)。
(2)硫化铝投入水中发生反应:Al2S3+6H2O====2Al(OH)3↓+3H2S↑,该反应___________(填“属于”或“不属于”)复分解反应。
(3)Ca(HCO3)2与Ca(OH)2反应属于复分解反应,写出反应的化学方程式__________ ;
(4)工业上可用氨与Cl2反应检验输送氯气的管道是否漏气,反应方程式如下:
8NH3+3Cl2====6NH4Cl+N2。
①请在上述方程式中表示出电子转移的方向和数目。
②该反应中,_________是还原剂;若反应中有1.5mol氧化剂参与反应,则发生转移的电子的物质的量为_______mol,被氧化的物质有__________mol。
(5)若将Cl2通入KI溶液中会发现无色溶液变成棕黄色后又褪色。这是因为发生如下2个反应: ①_____________; ②I2+Cl2+H2O=====HIO3+___________(不必配平)。
化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中发生了氧化还原反应的是( )

(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。

试写出有水参加、水为还原剂且为类型Ⅳ的一个化学方程式:_ _
(3)NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2的反应离子方程式是
![]() MnO4-+ NO2-+ ===== Mn2++ NO3-+ H2O
MnO4-+ NO2-+ ===== Mn2++ NO3-+ H2O
Ⅰ、请补充完整,配平方程式并标出电子转移方向和数目
Ⅱ、某同学称取了7.9 g KMnO4固体,欲配制100 mL溶液。回答下列问题:
该实验中,使用容量瓶时要检查是否漏水,其操作是: 。
Ⅲ、不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小 (请填序号) :
① 在溶解过程中有少量液体溅出烧杯外
② 定容时仰视仪器上的刻度线
③ 定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线
IV、最后所得的溶液应存放在试剂瓶中,并贴上标签,请你填写该标签(如图)。

V、某同学用上述配好的KMnO4溶液滴定末知浓度的NaNO2溶液:
取20mL末知浓度的NaNO2溶液于锥形瓶;
取上述配好的KMnO4溶液于 (“酸式”或“碱式”)滴定管
滴定完成后消耗KMnO4溶液10mL则NaNO2溶液的浓度为
查看习题详情和答案>>复分解反应和氧化还原反应都是重要的反应类型.回答下列问题:
(1)“盐+酸-→新盐+新酸”是复分解反应中的一种类型.在Na2SiO3溶液中滴入盐酸,生成的新酸是________(写化学式).
(2)硫化铝投入水中发生反应:Al2S3+6H2O![]() 2Al(OH)3↓+3H2S↑,该反应________(填“属于”或“不属于”)复分解反应.
2Al(OH)3↓+3H2S↑,该反应________(填“属于”或“不属于”)复分解反应.
(3)Ca(HCO3)2与Ca(OH)2反应属于复分解反应,写出反应的化学方程式________;
(4)工业上可用氨与Cl2反应检验输送氯气的管道是否漏气,反应方程式如下:
8NH3+3Cl2![]() 6NH4Cl+N2
6NH4Cl+N2
①请在上述方程式中表示出电子转移的方向和数目.
②
该反应中,________是还原剂;若反应中有1.5 mol氧化剂参与反应,则发生转移的电子的物质的量为________mol,被氧化的物质有________mol.(5)若将Cl2通入KI溶液中会发现无色溶液变成棕黄色后又褪色.这是因为发生如下2个反应:
①________;
②I2+Cl2+H2O![]() HIO3+
HIO3+

回答下列问题:
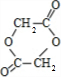
(1)环氧乙烷(
 )的结构可简写为
)的结构可简写为 则E的分子式是
则E的分子式是(2)写出结构简式:B



(3)G→I的反应类型是
(4)写出下列转化的化学方程式:C→K
| Cu |
| △ |
| Cu |
| △ |
| 水 |
| △ |
| 水 |
| △ |
(5)芳香烃族化合物Q(C9H10O4)充分加氢的产物为L,L与A的相对分子质量相同.Q有多种同分异构体,请写出两种符合下列条件的Q的同分异构体(已知:一个碳原子上连接两个-OH是不稳定结构)
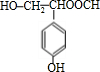

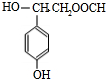

a 能与银氨溶液反应且能够水解
b 遇FeCl3溶液能发生显色反应
c 1molQ可与足量的Na反应生成标准状况下的H222.4L
d Q分子中苯环有两个取代基,且苯环上的一溴代物有2种.