网址:http://m.1010jiajiao.com/timu_id_193980[举报]
1
2
3
4
5
6
7
8
9
C
C
B
D
B
D
B
C
D
10
11
12
13
14
15
16
17
18
D
C
D
B
B
D
B
B
A
19
20
21
22
23
24
25
――
――
A
B
D
B
C
C
A
26、(14分)
⑴电解池 ,原电池 (2分,各1分)
2H2O+2CuSO4 = 2Cu+O2↑+2H2SO4 (5分,第一空1分,其它各2分)
(3)0.02 ,增加 ,0.63 , 1 。(7分,第二空1分,其它各2分)
27、(10分)
(1)Fe3++3H2O Fe(OH)3+3H+ ,将FeCl3先溶于盐酸,然后再加水稀释 。
Fe(OH)3+3H+ ,将FeCl3先溶于盐酸,然后再加水稀释 。
碳酸钙消耗了H+,使Fe3+水解程度增大,形成Fe(OH)3沉淀。(6分,各2分)
(2)白色悬浊液逐渐转变为黑色悬浊液。2AgCl(s)+S2―=Ag2S(s)+2Cl―。(4分,各2分)
28.(9分)
(1)增大 (2分)(2) 15―20min、25―30min 。(2分)
(3) 增大氧气的浓度,a、b。(3分,第二空2分,多选不给分)
(4)不 、向左。(2分,各1分)
29.(11分)
(1)①转移,定容 ②烧杯(或表面皿)、药匙。(4分,各1分)
(2)①溶液从无色恰好变为红色,且半分钟内不褪去。
②0.11mol?L-1 ③ 丙 ④ D (7分,第三空1分,其它各2分)
30.(6分)(1)0.04 mol?L-1?min-1、80% (2)16%
(算出反应速率且过程正确的给4分,转化率和体积分数各给1分)
实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。请完成填空:
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)转移→洗涤(并将洗涤液移入容量瓶)→ →将配制好的溶液倒入试剂瓶中,贴上标签。
②称量 g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、 。
(2)取20.00 mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
|
实验编号 |
NaOH溶液的浓度(mol/L) |
滴定完成时, NaOH溶液滴入的体积(mL) |
待测盐酸溶液的体积(mL) |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |
①滴定达到终点的标志是 。
②根据上述数据,可计算出该盐酸的浓度约 (保留两位有效数字)。
③排去碱式滴定管中气泡的方法应采用如图所示操作中的 (选择甲、乙、丙之一),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
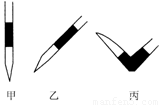
④ 在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有: 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.滴定过程中,有少量标准液溅出锥形瓶外。
E.碱式滴定管尖嘴部分有气泡,滴定后消失
查看习题详情和答案>>
实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。请完成填空:
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)转移→洗涤(并将洗涤液移入容量瓶)→ →将配制好的溶液倒入试剂瓶中,贴上标签。
②称量 g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、 。
(2)取20.00 mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
| 实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时, NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是 。
②根据上述数据,可计算出该盐酸的浓度约 (保留两位有效数字)。
③排去碱式滴定管中气泡的方法应采用如图所示操作中的 (选择甲、乙、丙之一),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
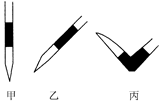
④ 在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有: 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.滴定过程中,有少量标准液溅出锥形瓶外。
E.碱式滴定管尖嘴部分有气泡,滴定后消失 查看习题详情和答案>>
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)转移→洗涤(并将洗涤液移入容量瓶)→ →将配制好的溶液倒入试剂瓶中,贴上标签。
②称量 g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、 。
(2)取20.00 mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
| 实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时, NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是 。
②根据上述数据,可计算出该盐酸的浓度约 (保留两位有效数字)。
③排去碱式滴定管中气泡的方法应采用如图所示操作中的 (选择甲、乙、丙之一),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
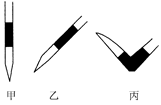
④ 在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有: 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.滴定过程中,有少量标准液溅出锥形瓶外。
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(14分)实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸的浓度的实验:请完成下列填空:
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→ (冷却后)→洗涤(并将洗涤液移入容量瓶)
→ → →将配制好的溶液倒入试剂瓶中,贴上标签。?
②称量 g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液
NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。?
| 实验编号 | NaOH溶液的浓度?(mol/L) | 滴定完成时, NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.76 | 20.00 |
①滴定达到终点的标志是 。
②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)。?
 ③排去碱式滴定管中气泡的方法应采用如图所示操作中的 ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
③排去碱式滴定管中气泡的方法应采用如图所示操作中的 ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
④在上述实验中,下列操作(其他操作正确)会造成测定结
果偏高的有 。
A.滴定终点读数时俯视读数 B.酸式滴定管使用前,水洗后未用待测盐酸润洗?
C.锥形瓶水洗后未干燥 D.称量NaOH固体中混有Na2CO3固体?
E.碱式滴定管尖嘴部分有气泡,滴定后消失
查看习题详情和答案>>有一未知浓度的食醋,某学生为测定CH3COOH的浓度在实验室中进行如下实验。请完成下列填空:
(1)配制100 mL 0.10 mol·L-1NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)________→洗涤(并将洗涤液移入容量瓶)→________→________→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量0.4 g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、________、________。
(2)取20.00 mL待测食醋放入锥形瓶中,由于食醋颜色较深,我们先____________________________________,并滴加2~3滴________做指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
|
实验 编号 |
NaOH溶液的浓度/(mol·L-1) |
滴定完成时,NaOH溶液滴入的体积/mL |
待测CH3COOH溶液的体积/mL |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |
①滴定达到终点的标志是
________________________________________________________________________。
②根据上述数据,可计算出该食醋中CH3COOH的浓度约为________(保留两位有效数字)。
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________。
A.滴定终点时俯视读数
B.移液管水洗后未用食醋溶液润洗
C.锥形瓶水洗后未干燥
D.称量前NaOH固体中混有Na2CO3固体
E.配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F.碱式滴定管尖嘴部分有气泡,滴定后消失
查看习题详情和答案>>
