网址:http://m.1010jiajiao.com/timu_id_172727[举报]
一、选择题(每小题只有一个正确答案,本题共54分)
1
2
3
4
5
6
7
8
9
C
B
B
A
D
D
B
B
C
10
11
12
13
14
15
16
17
18
C
A
B
B
A
C
C
C
A
(注:下列分值除注明的方程式3分之外,其他方程式每个2分,每空1分。)
二、填空题(26分)
19.(1)7;K2O、K2O2(KO2也可以)。
(2) (3)S2->Cl->Mg2+>Al3+
(3)S2->Cl->Mg2+>Al3+
(4)Na (5)H2O ;SiH4
(6)HS- +H3O+ = H2S +H2O HS-+OH- = S2-+H2O
20.(1)5
K
(2)C CO2
(3)5
21.(1)PCl3
(2) P(s)+Cl2(g)=== PCl3(g);△H=-306kJ?mol-1 (3分)
(3) PCl5(g)===PCl3(g)+Cl2(g);△H=+93kJ?mol-1 (3分)
(4)PCl5+4H2O===H3PO4+5HCl。
三、推断题(15分)
22.(1)(1)甲: Al2(SO4)3 ,乙:K2CO3 ,丙:AgNO3 ,丁:BaCl2,戊:NH4Br
(2)2Al3++3CO32-+3H2O==2Al(OH)3↓+3CO2↑
23.CaCl2 电子式:略; HClO4 HF
(2)SiO2 + 4HF = SiF4 + 2H2O
四、实验题(9分)
 (1)4H++2Cl─+MnO2 Mn2++Cl2↑+2H2O
(1)4H++2Cl─+MnO2 Mn2++Cl2↑+2H2O
(2)干燥管;除去氯气中的氯化氢
(3)使密度较大的氯气与密度较小的氨气能较快地均匀混合
(4)3Cl2+8NH3 ==N2+6NH4Cl b/2 amol-1
(5)在G连接导管,直接把尾气通入盛有烧碱溶液的烧杯中。
五、计算题(6分)
(1)2片小苏打所含NaHCO3的质量为
其物质的量为
由HCO3-+H+=== CO2↑+H2O,可知n(H+)=0.012mol。
(2)6片小苏打的物质的量为:0.036mol,即中和的H+为0.036mol,而每片的Al(OH)3
的物质的量为
中和的H+为0.009mol,所以Al(OH)3的片数为:0.036÷0.009 = 4片。
实验室中所用少量氯气用下列装置制取:
 |
试回答下列问题:
(1)写出该反应的离子方程式 。在该氧化还原反应中, HCl的作用是 。
(2)集气瓶B中盛装的是 。
(3)集气瓶C中盛装的是FeCl2溶液。实验开始后,C中反应的离子方程式为
。实验室中可用 检验反应生成的阳离子。在实验室也可用此反应的生成物来制备氢氧化铁胶体,请写出相应的化学方程式 。
(4)集气瓶D中盛装的是水,E装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 E中反应的化学方程式 。
(5)在F处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是
。
(6)若将F处的烧杯中的溶液改为澄清的石灰水,反应过程中的现象为 (选填标号)。
A.有白色沉淀 B.无现象 C.先生成白色沉淀而后消失
(7)氯气尾气直接排入大气中,会污染环境。实验室中可采用 来吸收有毒的氯气。该反应的离子方程式为 。
查看习题详情和答案>>
实验室中所用少量氯气用下列装置制取:
 |
试回答下列问题:
(1)写出该反应的离子方程式 。在该氧化还原反应中, HCl的作用是 。
(2)集气瓶B中盛装的是 。
(3)集气瓶C中盛装的是FeCl2溶液。实验开始后,C中反应的离子方程式为
。实验室中可用 检验反应生成的阳离子。在实验室也可用此反应的生成物来制备氢氧化铁胶体,请写出相应的化学方程式 。
(4)集气瓶D中盛装的是水,E装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 E中反应的化学方程式 。
(5)在F处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是
。
(6)若将F处的烧杯中的溶液改为澄清的石灰水,反应过程中的现象为 (选填标号)。
A.有白色沉淀 B.无现象 C.先生成白色沉淀而后消失
(7)氯气尾气直接排入大气中,会污染环境。实验室中可采用 来吸收有毒的氯气。该反应的离子方程式为 。
查看习题详情和答案>>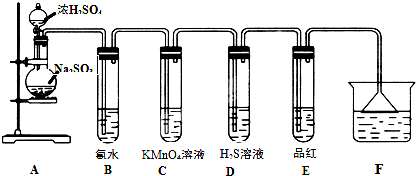
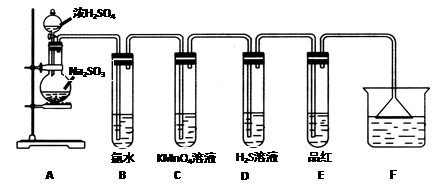
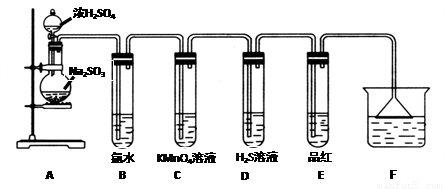
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是
(2)反应后,装置B中发生的现象是
(3)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
(4)F装置的作用是