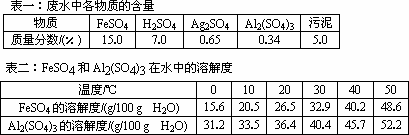
摘要:2 该课题组根据表中数据.设计了污水处理方案.拟利用该厂的废铁屑.烧碱溶液和硫酸处理此污水.回收FeSO4?7H2O和Ag. (1)请填写下列空白.完成得到Ag的实验方案:①将有锈斑的废铁屑先后用热的烧碱溶液和热水进行洗涤.目的是 ,②将工厂废水过滤.用少量水洗涤滤渣.洗涤液并入滤液后保留待用,③ .目的是使Ag+全部还原为金属Ag,④ .目的是分离出Ag, (2)请写出后续的步骤.除去Al3+.得到比较纯净的FeSO4?7H2O晶体:⑤将第 步与第④步所得滤液混合后.加入少量硫酸至混合液的pH为3~4. 滤出FeSO4?7H2O晶体,⑥ 得到较纯净的FeSO4?7H2O晶体. (3)步骤②中能否用变通自来水洗涤滤渣? .理由是 (4)步骤③中有关化学反应的离子方程式是 (5)在步聚⑤中.加少量硫酸调整pH的目的是 .
网址:http://m.1010jiajiao.com/timu_id_116475[举报]
1.(16分)
(1)①洗去油污(1分);③在②的滤液中加入稍过量的洗涤过的废铁屑,充分反应后过滤(1分);④将③的滤渣溶入足量的稀硫酸中,过滤,滤液保留待用(1分);(2)⑤、③(1分),将溶液加热到
(3)否(1分),普通自来水中含Cl―,使Ag+被沉淀(1分)。 (共2分)
(4)Fe+2Ag+
Fe2++2Ag,Fe2O3+6H+ 2Fe3++3H2O,Fe+2Fe3+ 3Fe2+,
Fe+2H+ Fe2++H2↑
(各1分,共4分)
(5)抑制Fe2+的水解,防止Fe2+被氧化 (2分)
2.(10分)(1)MnO2, NaOH溶液 (各1分) (共2分)
(2)2NaOH+Cl2==== NaCl+NaClO+H2O (2分)
(3)①不能(1分),HCl气体进入C中,消耗NaOH, 降低NaClO的纯度。(2分)(共3分)