网址:http://m.1010jiajiao.com/timu_id_11616[举报]
一、选择题(3×16=48分)
1.C 2.D 3.C 4.B 5.C 6.D 7.A 8.A 9.A 10.D 11.C 12.B 13.C 14.A 15.D 16.D
二、(5+7+6=18分)
17.(6分)
(1)结构 性质 用途 制法(2分);结构特点(1分)
(2)BD(3分,选1个得1分,错选得0分)
18.(第二空1分,其余每空2分,共7分)
2Clˉ-2e- = Cl2↑ 升高
阻止气体分子和某些离子通过,防止氢气和氯气混合发生爆炸,并能避免氯气和氢氧
化钠溶液作用生成次氯酸钠而影响烧碱的质量
NaCl +H2O  NaClO + H2 ↑
NaClO + H2 ↑
或 2 NaCl + 2 H2O
 H2↑ +
Cl2↑+
2NaOH
H2↑ +
Cl2↑+
2NaOH
Cl2 + 2NaOH ==== NaCl + NaClO + H2O
19.(6分)
(1)接触室(1分);热交换器(1分);使反应生成的热传递给进入接触室需预热的炉气,同时冷却生成的气体(1分)
(2)
(3)小于 (1分)
三、(12+10=22分)
20.(12分)
(1)Na+[∶H]-(2分)
??(2)阳极:4OH--4e-=O2↑+2H2O(2分)
???? 阴极:4Na++4e-=4Na(2分)
??(3)NaH+HCl=NaCl+H2↑(2分)
??(4)H2、Cl2、NaOH、HCl (4分)
21. (10分)
(1)N2H4(1)+O2(g)=N2(g)+2H2O;△H=-624kJ/mol(2分)
(2)①Cu2++2e-=Cu(2分) ②112 (2分)
(3)ClO-+2NH3=N2H4+Cl-+H2O(2分)
(4)N2+6H++6e-==2NH3 (2分)
四、(14分)
22.(14分)
方案Ⅰ:偏低(1分)
方案Ⅱ:①托盘天平(砝码)、药匙、酸式和碱式滴定管、锥形瓶(2分)
②B (1分)
③  (1分)
(1分)
方案Ⅲ:①保证CaCO3完全分解 (1分)
②应在干燥中冷却(1分)
方案Ⅳ:①A、B (2分)
②C (1分)
③偏高(1分)
方案Ⅱ(1分)
方案Ⅰ:气体体积难以准确测量(1分)
方案Ⅲ:实验室难以提供
五、计算(8分)
23. 1.13t(写出有关化学方程式或关系式4分)
(1)在进行性质实验方案的设计时,要充分了解物质的________、________、________和________之间的相互关系.要根据物质的________,设计实验方案来探索和验证物质所具有的一些性质.
(2)下列实验中所选用的仪器或操作以及结论不合理的是________
A、用托盘天平称量重11.7g氯化钠晶体
B、用碱式滴定管量取25.00mL溴水
C、不宜用瓷坩埚灼烧氢氧化钠、碳酸钠
D、测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
E、仅用蒸馏水和pH试纸作试剂,就可鉴别pH相等的H2SO4和CH3COOH溶液
(1)在进行性质实验方案的设计时,要充分了解物质的_______、_______、_______和______之间的相互关系。要根据物质的_______,设计实验方案来探索和验证物质所具有的一些性质。
(2)下列实验中所选用的仪器或操作以及结论不合理的是________
A.用托盘天平称量重11.7g氯化钠晶体
B.用碱式滴定管量取25.00mL溴水
C.不宜用瓷坩埚灼烧氢氧化钠、碳酸钠
D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
E.仅用蒸馏水和pH试纸作试剂,就可鉴别pH相等的H2SO4和CH3COOH溶液
查看习题详情和答案>>实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
(1)为了节约原料,硫酸和硝酸的最佳物质的量之比为________ ;为了吸收该反应中产生的尾气,可选择的最佳装置是________(填序号)。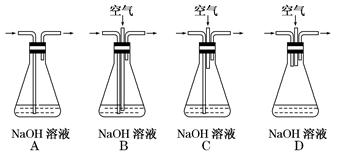
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计。
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再使氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与烯硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加入物质甲调节pH,铁元素全部转化为Fe(OH)3沉淀(一般当铁离子的浓度下降到10-5mol·L-1时,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:常温下,Ksp[Cu(OH)2]=10-22,Ksp[Fe(OH)3]=10-38)
请回答下列问题:
①方案1中仪器N的名称是________。
②方案2中为了使铁元素全部沉淀,应调节pH至少为________。
③方案2中甲物质可选用________(填序号)。
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
(1)为了节约原料,硫酸和硝酸的最佳物质的量之比为________ ;为了吸收该反应中产生的尾气,可选择的最佳装置是________(填序号)。
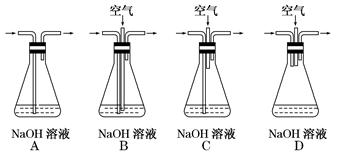
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计。
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再使氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与烯硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加入物质甲调节pH,铁元素全部转化为Fe(OH)3沉淀(一般当铁离子的浓度下降到10-5mol·L-1时,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:常温下,Ksp[Cu(OH)2]=10-22,Ksp[Fe(OH)3]=10-38)
请回答下列问题:
①方案1中仪器N的名称是________。
②方案2中为了使铁元素全部沉淀,应调节pH至少为________。
③方案2中甲物质可选用________(填序号)。
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末各组分均能被磁铁吸引。查阅资料得知:在温度不同、受热不均时会生成具有磁性的Fe3O4(组成相当于Fe2O3•FeO)。为进一步探究黑色粉末的组成及含量,他们进行了如下实验。
一.定性检验
(1)往黑色粉末中滴加盐酸,发现有气泡产生,则黑色粉末中一定有_ ___,产生气泡的离子方程式为____ 。
(2)热还原法检验:按下图装置连接好仪器(图中夹持设备已略去),检查装置的气密性。往装置中添加药品。打开止水夹K通人氢气,持续一段时间后再点燃C处的酒精灯。
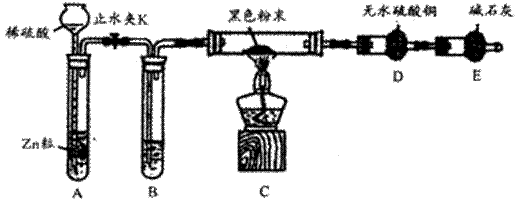
请回答下列问题:
①点燃C处酒精灯之前,为何要先持续通H2一段时间 。
②B中试剂的名称是_ 。
③若加热一段时间后,装置D中白色粉末变蓝色,对黑色粉末的组成得出的结论是 。
(3)为证明黑色粉末是否含Fe3O4,某同学还进行了如下实验:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,所得溶液分两份,第一份溶液滴入KSCN溶液,观察溶液是否变红;第二份溶液滴入酸性KMnO4溶液,观察酸性KMnO4溶液是否褪色。请回答:第一份溶液滴入KSCN溶液后一定会变红吗?请结合离子方程式简答 ;第二份溶液所进行的操作是欲检验溶液中是否存在 离子。经分析,你认为此方案是否可行 (填“是”或“否”)。
二.沉淀法定量测定
按如下实验流程进行测定:
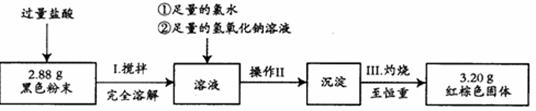
(4)操作II的名称是________ 、 ____ 、转移固体。
(5)通过以上数据,计算黑色粉末中各组分的物质的量之比为 。
查看习题详情和答案>>