题目内容
实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
(1)为了节约原料,硫酸和硝酸的最佳物质的量之比为________ ;为了吸收该反应中产生的尾气,可选择的最佳装置是________(填序号)。
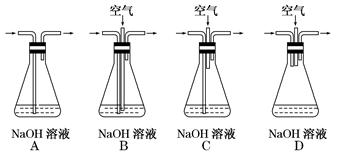
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计。
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再使氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与烯硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加入物质甲调节pH,铁元素全部转化为Fe(OH)3沉淀(一般当铁离子的浓度下降到10-5mol·L-1时,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:常温下,Ksp[Cu(OH)2]=10-22,Ksp[Fe(OH)3]=10-38)
请回答下列问题:
①方案1中仪器N的名称是________。
②方案2中为了使铁元素全部沉淀,应调节pH至少为________。
③方案2中甲物质可选用________(填序号)。
④方案2反应中加入少量FeSO4可加速铜的氧化,用离子方程式解释其原因:___________________________________________。
(1)为了节约原料,硫酸和硝酸的最佳物质的量之比为________ ;为了吸收该反应中产生的尾气,可选择的最佳装置是________(填序号)。

(2)为符合绿色化学的要求,某研究性学习小组进行如下设计。
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再使氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与烯硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加入物质甲调节pH,铁元素全部转化为Fe(OH)3沉淀(一般当铁离子的浓度下降到10-5mol·L-1时,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:常温下,Ksp[Cu(OH)2]=10-22,Ksp[Fe(OH)3]=10-38)
请回答下列问题:
①方案1中仪器N的名称是________。
②方案2中为了使铁元素全部沉淀,应调节pH至少为________。
③方案2中甲物质可选用________(填序号)。
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
(1)3∶2 B
(2)①坩埚 ②3.0 ③CD
④4Fe2++O2+4H+=4Fe3++2H2O、2Fe3++Cu=2Fe2++Cu2+
(2)①坩埚 ②3.0 ③CD
④4Fe2++O2+4H+=4Fe3++2H2O、2Fe3++Cu=2Fe2++Cu2+
(1)3Cu+3H2SO4+2HNO3=3CuSO4+2NO↑+4H2O,因此硫酸和硝酸的最佳物质的量之比为3∶2。NO与氢氧化钠溶液不反应,必须先使其与氧气反应生成NO2才能被氢氧化钠溶液吸收,故A错误,C、D的吸收效果不佳,最佳装置为B。(2)②c3(OH-)= =10-33,解得c(OH-)=10-11(mol·L-1),故pH=3.0。③根据Fe3++3H2O??Fe(OH)3+3H+,可加入 CuCO3、Cu2(OH)2CO3等促使平衡正向移动,从而生成氢氧化铁沉淀而除去Fe3+,并且不引入新杂质。
=10-33,解得c(OH-)=10-11(mol·L-1),故pH=3.0。③根据Fe3++3H2O??Fe(OH)3+3H+,可加入 CuCO3、Cu2(OH)2CO3等促使平衡正向移动,从而生成氢氧化铁沉淀而除去Fe3+,并且不引入新杂质。
 =10-33,解得c(OH-)=10-11(mol·L-1),故pH=3.0。③根据Fe3++3H2O??Fe(OH)3+3H+,可加入 CuCO3、Cu2(OH)2CO3等促使平衡正向移动,从而生成氢氧化铁沉淀而除去Fe3+,并且不引入新杂质。
=10-33,解得c(OH-)=10-11(mol·L-1),故pH=3.0。③根据Fe3++3H2O??Fe(OH)3+3H+,可加入 CuCO3、Cu2(OH)2CO3等促使平衡正向移动,从而生成氢氧化铁沉淀而除去Fe3+,并且不引入新杂质。
练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
 CO2 (g)+ H2 (g) △H<0,反应达到平衡后,为提高CO的转化率,可采取的措施有 ,已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中,c(H2O)﹕c(CO)不低于 ,
CO2 (g)+ H2 (g) △H<0,反应达到平衡后,为提高CO的转化率,可采取的措施有 ,已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中,c(H2O)﹕c(CO)不低于 ,

 =4,CO2的转化率随时间的变化关系如右图所示.
=4,CO2的转化率随时间的变化关系如右图所示.