网址:http://m.1010jiajiao.com/timu_id_115114[举报]
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的焓变(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
|
已知反应H2+I2═2HI,在一定条件下的数据如下,根据数据判断该反应是( )
|
(10分)由Fe2O3、CuO、A1中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):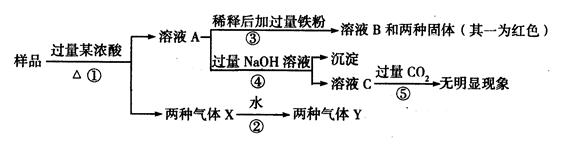
(1)混合气体Y中两种气体的化学式是 ,反应①中生成混合气体X的化
学方程式是 。
(2)通过上述实验及其现象说明,一定不含有的物质是 ,不能确定是否含有的物质是 ;
(3)为进一步确定样品中的未知物质,可以用上述反应过程中的溶液,设计一个简单的后续实验就可以确定,方法是 。
(10分)由Fe2O3、CuO、A1中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):
(1)混合气体Y中两种气体的化学式是 ,反应①中生成混合气体X的化
学方程式是 。
(2)通过上述实验及其现象说明,一定不含有的物质是 ,不能确定是否含有的物质是 ;
(3)为进一步确定样品中的未知物质,可以用上述反应过程中的溶液,设计一个简单的后续实验就可以确定,方法是 。
查看习题详情和答案>>
高铁酸钾(K2Fe04)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:
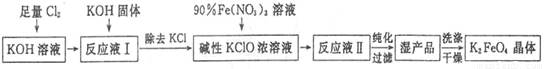
已知:2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)将Cl2通入KOH溶液中发生反应的离子方程式是____________。
(2)写出工业上制取Cl2的化学方程式____________。
(3)在“反应液I”中加入KOH固体的目的是____________。
(4)K2FeO4可作为新型多功能水处理剂的原因是____________。
(5)配制KOH溶液时,将61.6 g KOH固体溶解在100 mL水中,所得溶液的密度为 1.47 g • mL-1,则该溶液的物质的量浓度为____________。
(6)从“反应液II”中分离出K2Fe04后,副产品 是___________ (写 化 学 式)。
(7)该工艺每得到1.98kgK2FeO4,理论上消耗Cl2的物质的量为______mol。
查看习题详情和答案>>