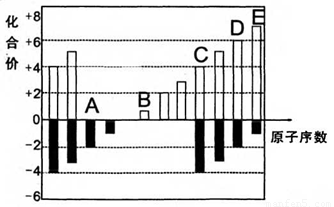
摘要:19.A.B.C.D.E均为短周期元素.且原子序数逐渐增大.A.D同主族.A与B的质子数之和等于C的质子数.A+离子与C2- 离子的核外电子数之和等于D+离子的核外电子数.B原子与D+离子的核外电子数之和等于E原子的核外电子数.(1).A.B.C.D.E的元素符号分别为 .(2).D.E元素可组成化合物甲.电解甲的水溶液时.反应的离子方程式为 ,A.C元素可组成原子个数比为1∶1的化合物乙.将E单质通入乙的水溶液中.生成一种强酸.并有气体放出.反应的化学方程式为 .(3)A.B.C.E中的任意三种元素可组成多种化合物.其中既含离子键又含共价键.且水溶液呈酸性的化合物有 .(4)A.C.D.E中的任意三种元素可组成多种化合物.其中溶于水时能抑制水电离的化合物有(各写一种不同类别的化合物) .它们能抑制水电离的理由是 .
网址:http://m.1010jiajiao.com/timu_id_113827[举报]
A、B、C、D、E均为短周期元素,其中A是形成化合物最多的元素;常温常压下,B元素形成的单质是淡黄色固体,常在火山口附近沉积;C和B同周期,且C的电负性大于B;D元素在地壳中含量最多;E元素的单质在空气中含量最多.
(1)C位于元素周期表第
(2)A、B、C三种元素的最高价氧化物对应水化物的酸性强弱由大到小的顺序是
(3)C的单质通入B的氢化物水溶液中,产生的实验现象是
(4)写出化合物AD2的电子式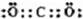
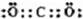 ,一种由D、E组成的化合物与AD2互为等电子体,其化学式为
,一种由D、E组成的化合物与AD2互为等电子体,其化学式为
查看习题详情和答案>>
(1)C位于元素周期表第
三
三
周期第ⅤⅡA
ⅤⅡA
族;合成E元素氢化物的工业反应化学方程式是H2+Cl2
2HCl
| ||
H2+Cl2
2HCl
.
| ||
(2)A、B、C三种元素的最高价氧化物对应水化物的酸性强弱由大到小的顺序是
HClO4>H2SO4>H2CO3
HClO4>H2SO4>H2CO3
(用相应酸的分子式表示).(3)C的单质通入B的氢化物水溶液中,产生的实验现象是
乳白色沉淀
乳白色沉淀
,发生反应的化学方程式Cl2+H2S═2HCl+S↓
Cl2+H2S═2HCl+S↓
.(4)写出化合物AD2的电子式
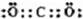
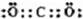
N2O
N2O
.A、B、C、D、E均为短周期元素,且原子序数逐渐增大.A、D最外层电子数相等且能形成离子化合物,A与B的质子数之和等于C的质子数,A+与 C2-的核外电子数之和等于D+离子的核外电子数,B 原子与 D+离子的核外电子数之和等于 E 原子的核外电子数.
(1)B的元素符号为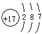
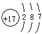 ;由A、C、E三种元素组成的化合物具有漂白性,其电子式为
;由A、C、E三种元素组成的化合物具有漂白性,其电子式为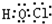
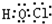 .
.
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
查看习题详情和答案>>
(1)B的元素符号为
N
N
,E的原子结构示意图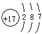
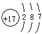
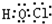
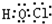
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
.(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
NH4NO3
NH4NO3
,物质乙抑制水的电离HNO3
HNO3
;室温下,若两溶液的pH都为4,则两溶液中水电离的氢离子浓度比为:甲:乙=106
106
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
>
>
7(填“>”“<”“=”),溶液中离子浓度由大到小的顺序为C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C(NH4+)>C(Cl-)>C(OH-)>C(H+)
.(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
H2+2e-+2OH-=2H2O
H2+2e-+2OH-=2H2O
.
A、B、C、D、E均为短周期元素,且原子序数依次递增。A、E同主族,B、D同周期,且B和D原子最外层电子数之和为10;A与D可形成A2D、A2D2型共价化合物。请回答下列问题。
(1)D在元素周期表中的位置是____________。
(2)E离子的结构示意图为____________。
(3)C2的电子式为____________,在E2D2中含有的化学键类型有____________。
(4)由A、B、C、D四种元素组成的离子化合物的化学式为(写出一种即可)____________。
查看习题详情和答案>>