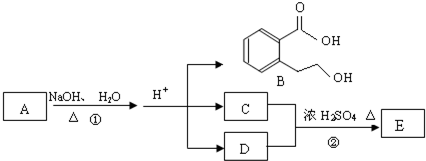
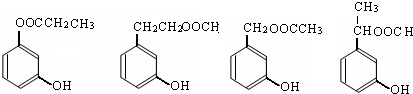
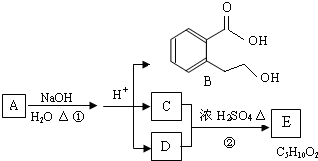
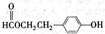题目内容
A、B、C、D、E均为短周期元素,且原子序数依次递增。A、E同主族,B、D同周期,且B和D原子最外层电子数之和为10;A与D可形成A2D、A2D2型共价化合物。请回答下列问题。(1)D在元素周期表中的位置是____________。
(2)E离子的结构示意图为____________。
(3)C2的电子式为____________,在E2D2中含有的化学键类型有____________。
(4)由A、B、C、D四种元素组成的离子化合物的化学式为(写出一种即可)____________。
(1)第2周期第ⅥA族
(2)![]()
(3)∶N┇┇N∶ 离子键、非极性键(或共价键)
(4)NH4HCO3〔或(NH4)2CO3〕
解析:短周期元素形成的A2D、A2D2型化合物,且A的原子序数小于D的只有H2O和H2O2,则A为H,D为O,与A(H)同主族且原子序数大于D(O)的E为Na,最外层电子数和D(O)最外层电子数之和为10且原子序数小于D(O)的B只能是C元素,原子序数介于B(C)与D(O)之间的C只能是N元素。依题意可作答。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目