30.配制一种质量分数为5%的氢氧化钠溶液50克:(1)计算需要氢氧化钠________克,水________毫升(水的密度为1 g/cm3);(2)氢氧化钠具有腐蚀性,易吸收空气中水分,使其表面潮湿最终溶解,所以在称量氢氧化钠固体时应放在___________里称量。在下表中用“√”表示你所选用的砝码,在下图中用“△”表示游码在标尺上的位置,以此表示你的称量过程(假设你所用的盛放氢氧化钠的容器质量为35.3克);(8分)
|
砝码(g) |
50 |
20 |
20 |
10 |
5 |
|
取用情况 |
|
|
|
|
|

(3)量取你所需要的水量,倒入盛放有氢氧化钠的烧杯里,用_______________搅拌,使氢氧化钠溶解,若此时你用手触摸烧杯外壁,你会感到__________________,原因是____
______________________________________________________。
(4)小明同学进行量取水量操作时,俯视刻度,那么用他量取的水配制溶液将会导致溶液中溶质的质量分数____________(填“偏大”、“偏小”或“不变”)。
29. 杜刚同学查阅有关资料得到:钠是一种非常活泼的金属,将其投入水中,它会漂在水面上与水发生剧烈反应,放出大量的热,使自身熔化成银白色的小球,甚至使生成的氢气燃烧,其反应的化学反应方程式为:2Na+2H2O=2NaOH+H2↑,但它不与煤油
杜刚同学查阅有关资料得到:钠是一种非常活泼的金属,将其投入水中,它会漂在水面上与水发生剧烈反应,放出大量的热,使自身熔化成银白色的小球,甚至使生成的氢气燃烧,其反应的化学反应方程式为:2Na+2H2O=2NaOH+H2↑,但它不与煤油
|
|
|


 杯里倒入一定量的水,向水中滴入2滴无色酚酞试液,再加入适量的
杯里倒入一定量的水,向水中滴入2滴无色酚酞试液,再加入适量的

 煤油,然后用小刀切一块绿豆般大的钠放入烧杯的水中,钠会悬浮于水
煤油,然后用小刀切一块绿豆般大的钠放入烧杯的水中,钠会悬浮于水
与煤油的界面处,并发生反应,直到钠消失,溶液变成红色。请你回答下列问题:
(1)反应生成的氢气在钠附近不会燃烧。其原因是___________________________________。
(2)由以上事实可以得出钠具有的物理性质有____________________、__________________
____________________、_____________________________。
(3)若反应的钠的质量为0.46克,则生成的氢气有__________________克。
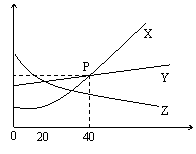
28.观察如图所示的X、Y、Z三种物质的溶解度曲线,回答问题:
|
(2)0℃~20℃时,X、Y、Z三种物质的溶解度大小
|
 (3)可以用升高温度、蒸发溶剂、加入溶质的方法
(3)可以用升高温度、蒸发溶剂、加入溶质的方法
|
(4)40℃时X的饱和溶液的溶质质量分数为_________;
(5)当X中混有少量Y时,可采取_____________________________方法提纯X。