28、辉铜矿的主要成分为Cu2S,是提取铜的主要原料。Cu2S在1200℃高温下被氧气氧化而发生如下反应:
2Cu2S+3O2→2Cu2O+2SO2 2Cu2O+Cu2S→6Cu+SO2
不考虑其他反应,(设空气中氮气和氧气的体积分数分别为0.80和0.20),试完成下列各题:
(1)1.0molCu2S氧化为Cu2O,需要标准状况下的空气的体积为_____L。
(2)1.0molCu2S与126升标准状况下空气反应,可生成Cu的物质的量____mol。
(3)1.0molCu2S与一定量空气反应,经分析得到固体混合物的含铜元素的质量分数为0.923,将固体物质的可能组成及相应的物质的量之比,填入下表(可不填满或补充)
|
物质的组成 |
相应的物质的量之比 |
|
|
|
|
|
|
|
|
|
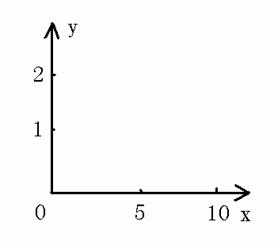 (4)1.0molCu2S与x mol空气反应,写出生成的Cu的物质的量(y)与x之间的函数关系,并在下图中画出y和x关系的图形。
(4)1.0molCu2S与x mol空气反应,写出生成的Cu的物质的量(y)与x之间的函数关系,并在下图中画出y和x关系的图形。
版权所有:()
版权所有:()
 上海交通大学附属中学2010-2011学年度第一学期
上海交通大学附属中学2010-2011学年度第一学期
 CH2=CHCH2-
CH2=CHCH2- -OH
-OH  -CH=CHCOOH
-CH=CHCOOH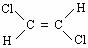 与
与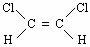 互为同分异构体(顺反异构),则化学式为C3H5Cl的链状的同分异构体有
( )
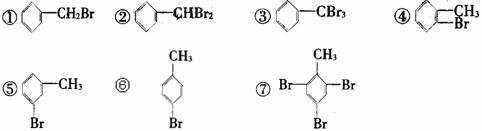
互为同分异构体(顺反异构),则化学式为C3H5Cl的链状的同分异构体有
( )
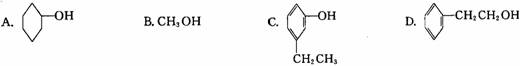
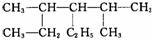 的物质,其名称是 ( )
的物质,其名称是 ( )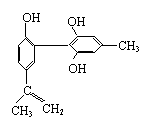 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是 ( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是 ( )