27.(14分)四种常见元素的性质或结构信息如下表,试根据信息回答有关问题。
|
元素 |
A |
B |
C |
D |
|
性质 结构 信息 |
原子核外有两个电子层,最外层有3个未成对的电子 |
原子的M层有1对成对的p电子K^S*5U.C#O |
有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
正三价阳离子的核外电子排布为[Ar]3d5 |
⑴写出B原子的电子排布式 。
⑵A元素的氢化物的沸点比同主族相邻元素氢化物沸点 (填“高”或“低”),其原因是 。
⑶D元素的某价态阳离子可与KCN溶液形成一种俗称黄血盐的配合物甲,甲的化学式可表示为K4[D(CN)6],则中心原子D的化合价为 ,甲在水溶液中的电离方程式为 ;已知D元素的另一种价态的离子可与KCN溶液形成另一种配合物乙,乙的配位数与甲相同,则乙的化学式为 。
 ⑷下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
⑷下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
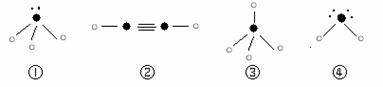
则在以上分子中,中心原子没有采用sp3杂化形成化学键的是 (填写序号);在②的分子中有 个σ键。高◎考※资*源
 (2)①铬
O=C=O ②H2CO3<H2SO4
③S>C>O
(2)①铬
O=C=O ②H2CO3<H2SO4
③S>C>O
26.(16分)下表为长式周期表的一部分,其中的编号代表对应的元素
|
① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
② |
③ |
④ |
⑤ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑥ |
|
|
⑧ |
⑦ |
|
|
|
|
|
|
|
⑨ |
|
|
⑩ |
|
|
|
|
|
|
|
⑾ |
|
试填空
(1)写出①、④两元素按原子个数比为1:1形成的化合物的电子式 ;写出上表中元素⑨原子的外围电子排布式 ;
(2)元素②与⑦形成的化合物的晶体类型是:_ _ _;
(3)元素⑤、⑥的第一电离能大小顺序是: > (用元素符号表示);元素③与元素①形成的X分子的空间构型为:
。请写出一种与N3-互为等电子体的分子的化学式

(4)⑦、⑧两种元素能形成一种AB2型的共价分子,该分子属于 分子(填“极性”或“非极性”)⑤、⑦、 ⑾三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素的单质。请写出⑦、⑾两种元素形成的互化物的化学式 (正价元素写在前面)。
(5)元素⑩在元素周期表分区中属于 区元素,元素⑩在一定条件下形成的晶体的两种晶胞如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为: 。

 NaHCO3+NaOH
NaHCO3+NaOH H2O+CH3COOC2H5
H2O+CH3COOC2H5