26、(8分)一般情况下,当人体一次性摄取300mg-500mg亚硝酸钠时,就会引起中毒。某研究小组用碘量法测定泡菜中亚硝酸盐的含量。有关反应如下:
2NaNO2 + 2H2SO4 +2KI = K2SO4 + I2 + 2H2O+ Na 2SO4 +2NO
I2 + 2 Na2S2O3 = 2 NaI + Na2S4O6
取1kg泡菜,榨汁,将榨出的液体收集后,加入提取剂和氢氧化钠,使得到的泡菜汁中的亚硝酸盐都成为要硝酸钠。在过滤后的滤液中加入氢氧化铝乳液,以除去色素。再次过滤后得到滤液,将该滤液稀释至1L,取25.00mL稀释后的滤液与过量的稀硫酸和碘化钾溶液反应,在选用合适的指示剂,用0.05000mol·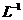
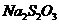 标准溶液进行滴定。实验数据记录如下;
标准溶液进行滴定。实验数据记录如下;
|
滴定次数 |
0.05000mol·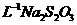 标准溶液体积/mL 标准溶液体积/mL |
|
|
滴定前刻度 |
滴定后刻度 |
|
|
1 |
0.00 |
20.04 |
|
2 |
0.12 |
20.08 |
|
3 |
0.05 |
20.05 |
请回答下列问题:
(1)该实验中可选用的指示剂是 ,滴定终点的现象是 。
(2)有经验的厨师在做泡菜时往往加入适量的橙汁,以减轻亚硝酸盐的危害。这主要是因为橙汁中含有丰富的维生素C,维生素C具有 性(填“氧化性”或“还原性”)
(3)通过计算判断若某人一次食入0.125kg这种泡菜,是否会引起中毒?
25、 (10分)二氧化锰是制造锌锰干电池的基本原料,普通锌锰干电池的电池反应式为:
(10分)二氧化锰是制造锌锰干电池的基本原料,普通锌锰干电池的电池反应式为:
 2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2。工业上以软锰矿为原料,利用硫酸亚铁制备高纯度二氧化锰的流程如下(软锰矿中所有金属元素在酸性条件下均以阳离子形式存在):
2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2。工业上以软锰矿为原料,利用硫酸亚铁制备高纯度二氧化锰的流程如下(软锰矿中所有金属元素在酸性条件下均以阳离子形式存在):
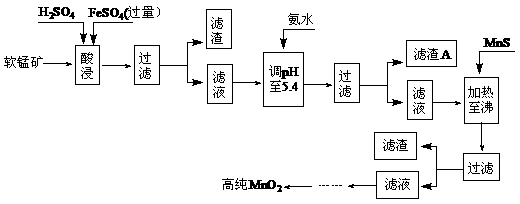










 某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.24%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物形式完全沉淀时,溶液的pH及部分硫化物的Ksp(均为25℃时)见下表,回答下列问题:
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.24%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物形式完全沉淀时,溶液的pH及部分硫化物的Ksp(均为25℃时)见下表,回答下列问题:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
|
pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
8.0 |
|
沉淀物 |
CuS |
ZnS |
MnS |
FeS |
|
|
|
Ksp |
8.5×10-45 |
1.2×10-23 |
1.4×10-15 |
3.7×10-14 |
|
|
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要化学方程式为:
 。
。
 (2)滤渣A的主要成分为
。
(2)滤渣A的主要成分为
。 (3)加入MnS的目的是除去
杂质。
(3)加入MnS的目的是除去
杂质。
 (4)碱性锌锰电池中,MnO2参与的电极反应式为
。
(4)碱性锌锰电池中,MnO2参与的电极反应式为
。
 (5)从废旧碱性锌锰电池中可回收利用的物质有
(写两种)
(5)从废旧碱性锌锰电池中可回收利用的物质有
(写两种)
24、(12分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请在右边方框内画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应 负极反应
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
|
提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢腐蚀。
有关反应的化学方程式
劣质不锈钢腐蚀的实验现象