30.(8分)Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+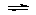 2Fe2++I2(水溶液),
2Fe2++I2(水溶液),
⑴该反应的平衡常数K的表达式为:K= ___________________________
[物质的浓度用“c(物质)”表示]。当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡________移动(填“向右”、“向左”、“不”)。
⑵上述反应的正向反应速率和I-、Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+)]n(其中K为常数)
|
|
c(I-)(mol/L) |
c(Fe3+)(mol/L) |
v[mol/(L·s)] |
|
⑴ |
0.20 |
0.80 |
0.032K |
|
⑵ |
0.60 |
0.40 |
0.144K |
|
⑶ |
 0.80 0.80 |
0.20 |
0.128K |
通过所给的数据计算得知:
 ①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为_________。
①在v=K[c(I-)]m[c(Fe3+)]n中,m、n的值为_________。
A. m=1、n=1 B. m=1、n=2 C. m=2、n=1 D. m=2、n=2
②I-浓度对反应速率的影响_______Fe3+浓度对反应速率的影响(填“>”、“<”或“=”)。
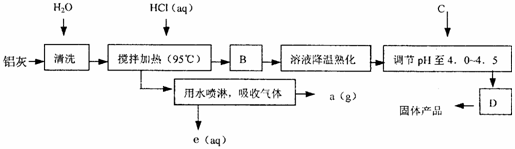
 (4)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。
(4)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。 。
。

 CH3COCH2I+H++I-。25℃时,该反应速率由下列经验式决定V=K c (CH3COCH3)c(H+),式中,k=2.73×10-5升/摩·秒。25℃时,已知反应开始时c(I2)=0.01摩/升,c(CH3COCH3)=0.1摩/升,c(H+)=0.02摩/升。求:
⑴反应开始时的速率_____________________。
CH3COCH2I+H++I-。25℃时,该反应速率由下列经验式决定V=K c (CH3COCH3)c(H+),式中,k=2.73×10-5升/摩·秒。25℃时,已知反应开始时c(I2)=0.01摩/升,c(CH3COCH3)=0.1摩/升,c(H+)=0.02摩/升。求:
⑴反应开始时的速率_____________________。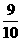 P,则VC=___,X___。
P,则VC=___,X___。