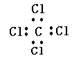14.(14分)密闭容器中,保持一定温度,进行如下反应:N2(g)+3H2(g)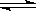 2NH3(g)。
2NH3(g)。
已知加入1mol N2和3mol H2,在恒压条件下,达到平衡时生成amol NH3[见下表中编号(1)的一行];在恒容条件下,达到平衡时生成b mol NH3[见下表中编号(4)的一行]。若相同条件下,达到平衡时混合物中各组分的百分含量不变,请填空:
|
状状 条件 |
起始时各物的物质的量(mol) |
平衡时NH3的物质量的量 (mol) |
||||
|
编号 |
x(N2) |
y(H2) |
z(NH3) |
|||
|
恒 压 |
(1) |
1 |
3 |
0 |
a |
|
|
(2) |
3 |
|
0 |
|
||
|
(3) |
|
|
0.2 |
0.5a |
||
|
x、y、z取值必须满足的一般条件:
。 |
||||||
|
恒 容 |
(4) |
1 |
3 |
0 |
b |
|
|
(5) |
0 |
0 |
|
b |
||
|
(6) |
|
2.25 |
|
b |
||
|
x、y、z取值必须满足一般条件(一个只含x、z,另一个只含y、z): ; 。 |
||||||
|
|
a与b的关系是:a
b(填>、<、=) |
|||||
12.双指示法可用来测定由NaOH、Na2CO3、NaHCO3中的一种或两种物质组成的混和物的含量。具体做法是:向待测液中加入酚酞,用标准盐酸滴定,当红色褪去,此时NaOH被完全中和,且Na2CO3转化为NaHCO3,消耗盐酸V1mL,然后者加甲基橙指示剂,用同一种盐酸继续滴定,当黄色变为橙色时,被转化为NaCl,消耗盐酸V2mL。
(1)判断物质的组成,请用Na2CO3、NaHCO3、NaOH填空
|
V的变化 |
V1≠0 V2=0 |
V1=0 V2≠0 |
V1>V2>0 |
V2>V1>0 |
|
试样的成分 |
|
|
|
|
(2)若盐酸的浓度为0.5mol/L,含惰性杂质的混和物的质量为1.25g,V1=30mL,V2=5mL,则各组分的百分含量是多少?