22.(8分)回答下列问题(填序号):
(1)下列仪器中:①漏斗 ②容量瓶 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥量筒⑦燃烧匙。
常用于物质分离的是 ,其中根据物质沸点不同来分离物质的仪器
是 。(用序号填写)
(2)今欲用NaOH固体配制500mL 0.2mol/L的NaOH溶液。根据题意填空:
A.配制该溶液应选用 mL容量瓶。
B.用托盘天平称取 g固体NaOH。
C.将称好的NaOH固体放至500mL的大烧杯中,倒入约250mL蒸馏水,用 搅拌至完全溶解。待冷却至室温后,将烧杯中的溶液用玻璃棒引流转移至容量瓶。
D.用少量蒸馏水洗涤烧杯2-3次,并将每次洗涤的溶液都注入容量瓶, 轻轻晃动容量瓶,使溶液混和均匀。
E.向容量瓶中加入蒸馏水,直到液面离刻度线约1-2厘米时,改用 滴加蒸馏水至液面与刻度线相切。盖好瓶塞,摇匀。如果加水时液面超过刻度线,将使配得的溶液浓度 (填“偏高”、“偏低”或 “无影响”)。
F.配制好的溶液 (填“能”或“不能”)长期存放在容量瓶中。
|
2FeSO4 ==== Fe2O3 +SO2↑+SO3↑ 为检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
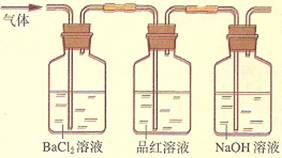
②将FeSO4高温分解产生的气体通入右图所示的装置中,以检验产生的气体中是否含有SO2和SO3。请回答以下问题:
(1)写出用KSCN检验Fe3+的离子方程式 。
(2)操作②中氯化钡溶液中的现象是 。品红溶液的作用是 ,品红溶液中可观察到现象是 。
(3)操作②中最后要将通过品红溶液的气体再通入NaOH溶液中,这样做的目的是
,氢氧化钠溶液中发生反应的化学方程式为 。
16.下列除杂所选用的试剂及操作方法均正确的一组是( )
|
选项 |
待提纯的物质 |
选用的试剂 |
操作方法 |
|
A |
NaOH(Na2CO3) |
盐酸 |
- |
|
B |
CO2(CO) |
CuO |
加热 |
|
C |
Fe (Al) |
稀硫酸 |
过滤 |
|
D |
CO2(HCl) |
Na2CO3溶液 |
洗气 |