37.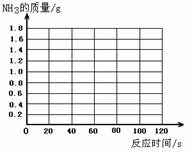 某校科学兴趣小组为测定某样品中氯化铵的质量分数,将6g样品溶于18g水后,再加入7.6g氢氧化钠浓溶液共热,两者恰好完全反应(样品中的杂质不与氢氧化钠反应,也不溶于水,氯化铵与氢氧化钠的反应方程式为:NH4Cl+NaOH △ NaCl+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液完全吸收,同时测量120秒内硫酸溶液增加的质量,结果如下表所示。
某校科学兴趣小组为测定某样品中氯化铵的质量分数,将6g样品溶于18g水后,再加入7.6g氢氧化钠浓溶液共热,两者恰好完全反应(样品中的杂质不与氢氧化钠反应,也不溶于水,氯化铵与氢氧化钠的反应方程式为:NH4Cl+NaOH △ NaCl+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液完全吸收,同时测量120秒内硫酸溶液增加的质量,结果如下表所示。
|
时间/s |
0 |
20 |
30 |
40 |
60 |
80 |
100 |
120 |
|
硫酸溶液增 加的质量/g |
0 |
0.7 |
1.0 |
1.2 |
1.5 |
1.6 |
1.7 |
1.7 |
试回答下列问题:
(1)请在右图中画出产生气体的质量随反应时间变化关系曲线;
 (2)样品中氯化铵的质量分数为 ▲ ;
(2)样品中氯化铵的质量分数为 ▲ ;
(3)求反应后所得氯化钠溶液的溶质质量分数(不考虑反应过程中水分的损失)。
35.同学们都有这样的学习和生活经验:夏天,将食品放在冰箱里不容易腐烂;木炭在氧气中燃烧比在空气中燃烧得更旺;颗粒状石灰石比块状石灰石与盐酸反应产生的气泡更快。说明反应物的浓度(溶质质量分数)、温度和固体反应物的表面积对化学反应快慢有影响。小明利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,下表是五组50mL稀硫酸与0.1g某金属反应的实验数据(丝状金属的规格相同):
|
实验序号 |
1 |
2 |
3 |
4 |
5 |
|
|
金属状态 |
丝状 |
粉末状 |
丝状 |
丝状 |
丝状 |
|
|
稀硫酸质量分数/% |
5 |
5 |
10 |
10 |
15 |
|
|
溶液温度/℃ |
反应前 |
20 |
20 |
20 |
35 |
丢失数据 |
|
反应后 |
34 |
35 |
35 |
50 |
55 |
|
|
金属消失的时间/s |
500 |
50 |
125 |
50 |
30 |
分析上述数据,回答下列问题:
(1) 比较实验 ▲ (填实验序号),表明反应物浓度越大,化学反应越快;
(2) 比较实验1和2,表明 ▲ ,化学反应越快;
(3) 依据实验规律,推测“丢失数据”的值约是 ▲ ℃。
34.某同学进行了如下实验:根据右图连接好实物,用电流表分别测出I、I1、I2的电流,改变电源电压,重复实验,记录数据如下表。
|
电流 次数 |
I1/A |
I2/A |
I/A |
|
1 |
0.2 |
0.2 |
0.4 |
|
2 |
0.3 |
0.3 |
0.6 |
|
3 |
0.4 |
0.4 |
0.8 |
(1)该实验探究的问题是 ▲ ;
(2)该同学根据实验得出结论:并联电路中干路电流为支路电流的2倍。该实验有不完善之处,请你提出改进的建议: ▲ 。
33.中央电视台曾介绍段儒斌发明的微生物催腐剂(含腐生细菌),微生物催腐剂的推广使用有助于解决由焚烧秸秆、稻草带来的环境污染、土地肥力下降等问题。小明为探究腐生细菌对植物落叶的分解作用,将经过灭菌处理的落叶分成甲、乙、丙三组,按下表设计,浇上等量的蒸馏水,放在无菌环境条件下进行培养,并得到如下实验现象:
|
组别 |
腐生细菌 |
温度/℃ |
实验现象 |
|
甲 |
无 |
25 |
第25天落叶还没变化 |
|
乙 |
有 |
25 |
第25天落叶完全腐烂 |
|
丙 |
有 |
35 |
第18天落叶完全腐烂 |
 (1)该实验的假设是 ▲ ;
(1)该实验的假设是 ▲ ;
(2)实验时,甲、乙、丙三组所取的落叶应满足的条件是 ▲ ;
(3)从实验中可得出的结论是: ▲ 。
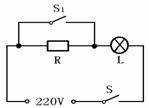 将“220V 40W”的灯泡、阻值为990Ω的电阻和开关S、S1连成如图所示的电路。天黒后,S处于闭合状态,当无人入厕时,开关S1断开,此时灯较暗,但能起到指示作用;当有人入厕时,闭合开关S1,灯泡正常发光,起到照明作用。
将“220V 40W”的灯泡、阻值为990Ω的电阻和开关S、S1连成如图所示的电路。天黒后,S处于闭合状态,当无人入厕时,开关S1断开,此时灯较暗,但能起到指示作用;当有人入厕时,闭合开关S1,灯泡正常发光,起到照明作用。 实验:将新制的氢氧化铜粉末放入试管中,使其在加热条件下分解(如右图),观察到蓝色粉末逐渐变成黑色。
实验:将新制的氢氧化铜粉末放入试管中,使其在加热条件下分解(如右图),观察到蓝色粉末逐渐变成黑色。