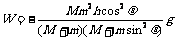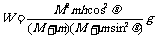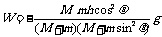22.(共8分,每空2分)衡水中学某实验小组在进行“验证动量守恒定律”的实验。入射球与被碰球半径相同。
① 实验装置如下图所示。先不放B球,使A球从斜槽上某一固定点C由静止滚下,落到位于水平地面的记录纸上留下痕迹。再把B球静置于水平槽前端边缘处,让A球仍从 C处由静止滚下,A球和B球碰撞后分别落在记录纸上留下各自落点的痕迹。记录纸上的O点是重锤所指的位置,M、P、N分别为落点的痕迹。

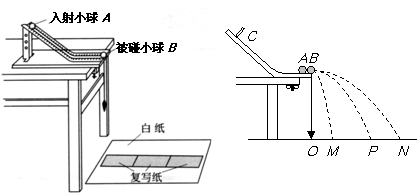
② 释放多次后,取各落点位置的平均值,测得各落点痕迹到O点的距离:OM=13.10cm,OP=21.90cm,ON=26.04cm。用天平称得入射小球A的质量m1=16.8g,被碰小球B的质量m2 = 5.6 g。若将小球质量与水平位移的乘积作为“动量”,请将下面的数据处理表格填写完整。(保留2位有效数字)
|
OP/m |
OM/m |
ON/m |
碰前总动量 p/ kg·m |
碰后总动量 p′/ kg·m |
相对误差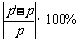 |
|
0.2190 |
0.1310 |
0.2604 |
3.68×10-3 |
|
|
根据上面表格中的数据处理数据,你认为能得到的结论是: 。
③ 完成实验后,实验小组对上述装置进行了如下图
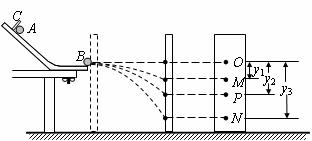 所示的改变:(I)在木板表面先后钉上白纸和复写纸,并将木板竖直立于靠近槽口处,使小球A从斜槽轨道上某固定点C由静止释放,撞到木板并在白纸上留下痕迹O;(II)将木板向右平移适当的距离固定,再使小球A从原固定点C由静止释放,撞到木板上得到痕迹P;(III)把半径相同的小球B 静止放在斜槽轨道水平段的最右端,让小球A仍从原固定点由静止开始滚下, 与小球B 相碰后,两球撞在木板上得到痕迹
M和 N;(IV)用刻度尺测量纸上O点到M、P、N 三点的距离分别为y1、y2、y3。请你写出用直接测量的物理量来验证两球碰撞过程中动量守恒的表达式:
。(小球A、B的质量分别为m1、m2)
所示的改变:(I)在木板表面先后钉上白纸和复写纸,并将木板竖直立于靠近槽口处,使小球A从斜槽轨道上某固定点C由静止释放,撞到木板并在白纸上留下痕迹O;(II)将木板向右平移适当的距离固定,再使小球A从原固定点C由静止释放,撞到木板上得到痕迹P;(III)把半径相同的小球B 静止放在斜槽轨道水平段的最右端,让小球A仍从原固定点由静止开始滚下, 与小球B 相碰后,两球撞在木板上得到痕迹
M和 N;(IV)用刻度尺测量纸上O点到M、P、N 三点的距离分别为y1、y2、y3。请你写出用直接测量的物理量来验证两球碰撞过程中动量守恒的表达式:
。(小球A、B的质量分别为m1、m2)
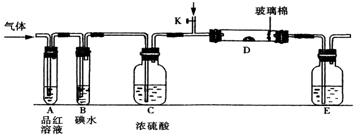 某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。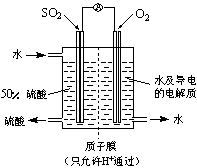 向含X的水溶液中加入稀硫酸时的现象是______________________________,发生反应的离子方程式为______________________________
向含X的水溶液中加入稀硫酸时的现象是______________________________,发生反应的离子方程式为______________________________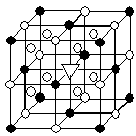 (3)R元素单原子形成的离子在水中不存在,Q单质与水作用可生成R的单质。由W、R、Z三种元素形成化合物溶于水显碱性,用离子方程式表示其原因
,Z、W、Q形成的化合物的化学式为W3ZQ6,其晶体结构单元如右图所示,已知该化合物熔融时电离方程式为W3ZQ6 =3W+ + ZQ63-,●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是_____(填序号A.W+ B.Z3+
(3)R元素单原子形成的离子在水中不存在,Q单质与水作用可生成R的单质。由W、R、Z三种元素形成化合物溶于水显碱性,用离子方程式表示其原因
,Z、W、Q形成的化合物的化学式为W3ZQ6,其晶体结构单元如右图所示,已知该化合物熔融时电离方程式为W3ZQ6 =3W+ + ZQ63-,●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是_____(填序号A.W+ B.Z3+
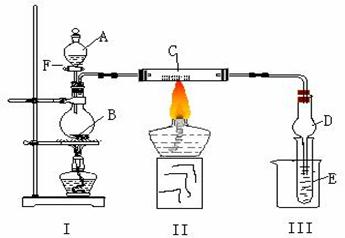
 (2)若I处酒精灯不加热,,B、C仍是实验(1)中原物质实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是
(写化学式),E中是
(写化学式)与葡萄糖的混合液。请写出反应管C中所发生反应的方程式
。
(2)若I处酒精灯不加热,,B、C仍是实验(1)中原物质实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是
(写化学式),E中是
(写化学式)与葡萄糖的混合液。请写出反应管C中所发生反应的方程式
。 (1)第一个铁块放上后,木板运动L=1m时,木板的速度多大?
(1)第一个铁块放上后,木板运动L=1m时,木板的速度多大?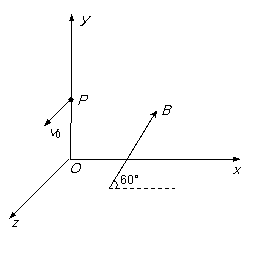
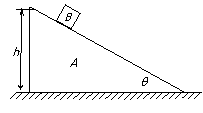
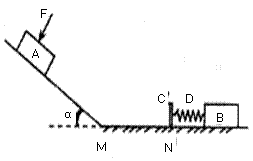 (16分)如图所示,粗糙斜面与水平面通过半径可忽略的光滑小圆弧平滑连接,斜面倾角α=37°,水平面的M到N段是长度L1=0.3m的粗糙平面,N点的右边是光滑的。A、B是两个质量均为m=1kg的小滑块(可看作质点),置于N点处的C是左端附有胶泥的薄板(质量不计),D是两端分别与B和C连接的轻质弹簧,滑块A与斜面和与水平面MN段的动摩擦因数相同。当滑块A置于斜面上且受到大小F=4N、方向垂直斜面向下的恒力作用时,恰能向下匀速运动。现撤去F,让滑块A从斜面上距斜面底端L2=1m处由静止下滑(取g=10m/s2,sin37°=0.6,cos37°=0.8),求:
(16分)如图所示,粗糙斜面与水平面通过半径可忽略的光滑小圆弧平滑连接,斜面倾角α=37°,水平面的M到N段是长度L1=0.3m的粗糙平面,N点的右边是光滑的。A、B是两个质量均为m=1kg的小滑块(可看作质点),置于N点处的C是左端附有胶泥的薄板(质量不计),D是两端分别与B和C连接的轻质弹簧,滑块A与斜面和与水平面MN段的动摩擦因数相同。当滑块A置于斜面上且受到大小F=4N、方向垂直斜面向下的恒力作用时,恰能向下匀速运动。现撤去F,让滑块A从斜面上距斜面底端L2=1m处由静止下滑(取g=10m/s2,sin37°=0.6,cos37°=0.8),求: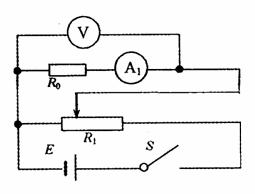 (共8分,每空2分)某课题研究小组,收集了数码相机、手机等用旧了各种类型的电池,及从废旧收音机上拆下的电阻、电容、电感线圈。现从这些材料中选取两个待测元件:一是电阻R0(约为2kΩ),二是手机中常用的锂电池(电动势E标称值为3.7V)。在操作台上还准备了如下实验器材:
(共8分,每空2分)某课题研究小组,收集了数码相机、手机等用旧了各种类型的电池,及从废旧收音机上拆下的电阻、电容、电感线圈。现从这些材料中选取两个待测元件:一是电阻R0(约为2kΩ),二是手机中常用的锂电池(电动势E标称值为3.7V)。在操作台上还准备了如下实验器材: (2)在实际操作过程中,发现滑动变阻器R1、电流表A1都已损坏无法使用,请用余下的实验器材(R0除外)测量锂电池的电动势E和内阻r。
(2)在实际操作过程中,发现滑动变阻器R1、电流表A1都已损坏无法使用,请用余下的实验器材(R0除外)测量锂电池的电动势E和内阻r。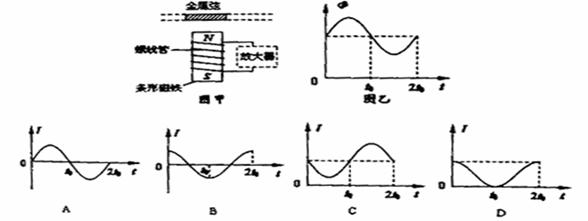
 B.
B.