0 123377 123385 123391 123395 123401 123403 123407 123413 123415 123421 123427 123431 123433 123437 123443 123445 123451 123455 123457 123461 123463 123467 123469 123471 123472 123473 123475 123476 123477 123479 123481 123485 123487 123491 123493 123497 123503 123505 123511 123515 123517 123521 123527 123533 123535 123541 123545 123547 123553 123557 123563 123571 447348
 右图曲线显示一个处于安静状态的人在不同气温中,
右图曲线显示一个处于安静状态的人在不同气温中, 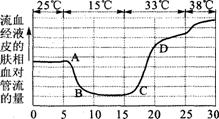 流经皮肤血管的血液相对流量。据此判断,下列叙述
流经皮肤血管的血液相对流量。据此判断,下列叙述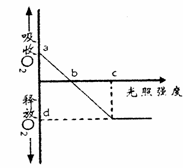 如右图为植物光合作用强度随光照强度变化的坐标曲线图,分析下列叙述,不正确的是( )
如右图为植物光合作用强度随光照强度变化的坐标曲线图,分析下列叙述,不正确的是( ) 

 下图表示人体通过体液免疫消灭破伤风杆菌外毒素的过程,下列相关叙述正确的是
下图表示人体通过体液免疫消灭破伤风杆菌外毒素的过程,下列相关叙述正确的是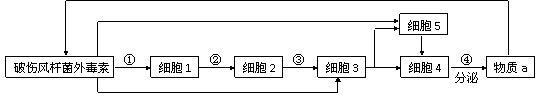
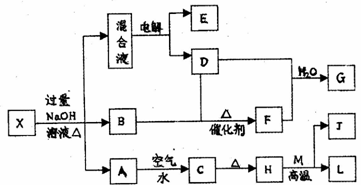
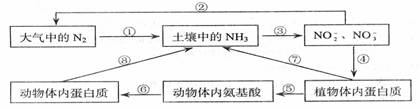 下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是( )
下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是( )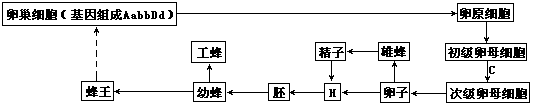
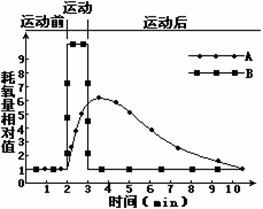 Ⅰ.(10分)图中曲线A表示某人在短时间内剧烈运动及其前后的实际耗氧量,曲线B是根据其运动量大小计算出的耗氧量理论值,请据图回答:⑴在2min-3min时,曲线A大大低于曲线B,这是因为人体此时能量的供应来自于
Ⅰ.(10分)图中曲线A表示某人在短时间内剧烈运动及其前后的实际耗氧量,曲线B是根据其运动量大小计算出的耗氧量理论值,请据图回答:⑴在2min-3min时,曲线A大大低于曲线B,这是因为人体此时能量的供应来自于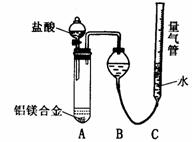 (12分)铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
(12分)铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。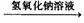 测定剩余固体质量
测定剩余固体质量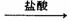 测定生成气体的体积
测定生成气体的体积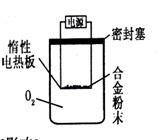 (2)为准确测定生成气体的体积,实验中应注意的问题是(只要求写出其中一点):
(2)为准确测定生成气体的体积,实验中应注意的问题是(只要求写出其中一点):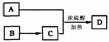 所示转化关系 ,D的分子式为C10H12O3
,
所示转化关系 ,D的分子式为C10H12O3
,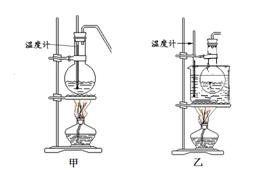 (5)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290°C,熔点18.17°C),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。 甲、乙两装置比较,乙装置有哪些优点
(5)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290°C,熔点18.17°C),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。 甲、乙两装置比较,乙装置有哪些优点