33.(16分)苄佐卡因是一中医用麻醉药品,学名对氨基苯甲酸乙酯,它以对硝基甲苯为主要起始原料经下列反应制得:
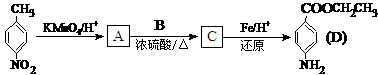
请回答下列问题:








(1)写出A、B、C的结构简式:A 、B 、C 。
(2)用1H核磁共振谱可以证明化合物C中有 种氢原子处于不同的化学环境。
(3)写出同时符合下列要求的化合物C的所有同分异构体的结构简式(E、F、G除外)
①化合物是1,4-二取代苯,其中苯环上的一个取代基是硝基
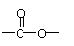
②分子中含有 结构的基团
注:E、F、G结构如下:
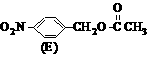 、
、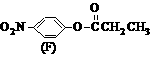 、
、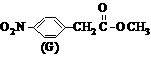 。
。
(4)E、F、G中有一化合物经酸性水解,其中的一种产物能与FeCl3溶液发生显色反应,写出该水解反应的化学方程式 。
(5)苄佐卡因(D)的水解反应如下:
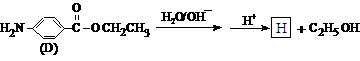
化合物H经聚合反应可制成高分子纤维,广泛用于通讯、导弹、宇航等领域。请写出该聚合反应的化学方程式 。
34 (3个小题18分)








(1)在做“互成角度的两个共点力的合成”的实验中有以下实验步骤,其合理顺序是: 。(用相应字母表示)
A.通过改变两个拉力的大小和方向,从而改变橡皮条的伸长,再重复做几次;
B.只用一个弹簧秤,通过细绳把橡皮条的结点拉到同样的位置O,记下弹簧秤的读数和细绳的方向,按同样比例作出这个力F’的图示;
C.在桌面上放一块方木板,在木板上垫一张白纸,把橡皮条一端固定在木板的 A点;
D.记下两个弹簧秤的读数以及结点的位置,描下两条细绳的方向,在纸上按比例作出力F1和F2的图示,用平行四边形定则求出(作出)合力F;
E.比较力F’与用平行四边形定则求出的力F,看它们在实验误差范围内是否相等;
F.用两条细绳结在橡皮条的另一端(即结点),通过细绳用两个弹簧秤互成角度拉橡皮条,橡皮条伸长,使结点到达某一位置O;
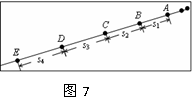
(2)(12分)一小球沿光滑斜面向下运动,用每隔0.1s曝光一次的频闪照相机拍摄下不同时刻小球的位置照片如图7所示,选小球的五个连续位置A、B、C、D、E进行测量,测得距离s1、s2、s3、s4的数据如表格所示。(计算结果保留三位有效数字)
|
s1(cm) |
s2(cm) |
s3(cm) |
s4(cm) |
|
8.20 |
9.30 |
10.40 |
11.50 |
根据以上数据可知小球沿斜面下滑的加速度的大小为______m/s2(6分)
根据以上数据可知小球在位置A的速度时______m/s,位置D的速度时______m/s。(6分)
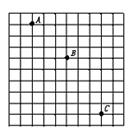
(3)如图所示为一小球做平抛运动的闪光照相照片的一部分,图中背景方格的边长均为5cm.如果取g=10m/s2,那么,(1)闪光频率是_______Hz.(2)小球运动中水平分速度的大小是________m/s.(3)小球经过B点时的速度大小是________m/s.
 (
(
31.(16分)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO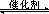 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/mol·L-1 |
1.00×10-3 |
4.50×10-4 |
2.50×10-4 |
1.50×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)/ mol·L-1 |
3.60×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):








(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)在该温度下,反应的平衡常数K= 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
|
实验编号 |
T/℃ |
NO初始浓度/ mol·L-1 |
CO初始浓度/mol·L-1 |
催化剂的比表面积/
m2·g-1 |
|
Ⅰ |
280 |
1.20×10-3 |
5.80×10-3 |
82 |
|
Ⅱ |
|
|
|
124 |
|
III |
350 |
|
|
124 |
①请在上表格中填入剩余的实验条件数据。
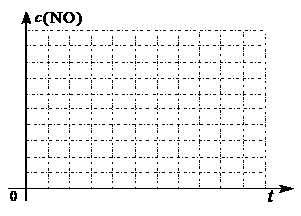
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线是实验编号。
30.(16分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题: 








 族 族周期 |
ⅠA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序是 ,⑧的阴离子结构示意图为 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号) 。
a.MnO2 b.FeCl3 C.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
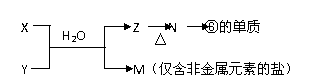

X溶液与Y溶液反应的离子方程式为 ,N→⑥的单质的化学方程式为 ,常温下,为使0.1mol/L M溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至 。
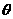 =37°,一质量M=10kg物体,在斜面底部受到一个沿斜面向上的F=100N的力作用由静止开始运动,物体在2s内位移为4m,
=37°,一质量M=10kg物体,在斜面底部受到一个沿斜面向上的F=100N的力作用由静止开始运动,物体在2s内位移为4m,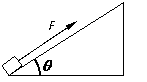 (1)物体与斜面间的动摩擦因数
(1)物体与斜面间的动摩擦因数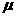 ;
; 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
移动(填“向左”“向右”或“不”);使用催化剂 反应的△H(填“增大”“减小”或“不改变”),原因是
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
移动(填“向左”“向右”或“不”);使用催化剂 反应的△H(填“增大”“减小”或“不改变”),原因是
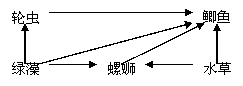 (16分)右图为有5个物种构成的食物网,如图所示,且该生态系统在没有人为干扰的情况下达到相对稳定平衡状态。请据图回答:
(16分)右图为有5个物种构成的食物网,如图所示,且该生态系统在没有人为干扰的情况下达到相对稳定平衡状态。请据图回答: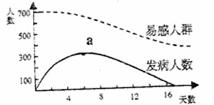 (2)某地对一段时间内流感发病情况作了统计(见右图)。
(2)某地对一段时间内流感发病情况作了统计(见右图)。 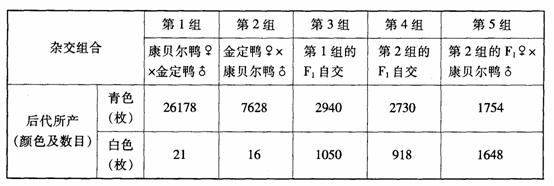
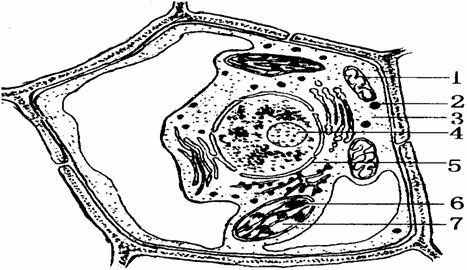
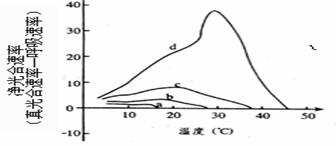 (6)若该细胞为马铃薯,下图中4条曲线(a、b、c、d)为不同光照强度和不同CO2浓度下,马铃薯净光合速率随温度变化的曲线。a光照非常弱,CO2很少(远小于0.03%);b适当遮荫(相当于全光照的1/25)CO2浓度为0.03%,c全光照(晴天不遮荫),CO2浓度为0.03%;d全光照,CO2浓度为1.22%。请据图回答:
(6)若该细胞为马铃薯,下图中4条曲线(a、b、c、d)为不同光照强度和不同CO2浓度下,马铃薯净光合速率随温度变化的曲线。a光照非常弱,CO2很少(远小于0.03%);b适当遮荫(相当于全光照的1/25)CO2浓度为0.03%,c全光照(晴天不遮荫),CO2浓度为0.03%;d全光照,CO2浓度为1.22%。请据图回答: