0 10162 10170 10176 10180 10186 10188 10192 10198 10200 10206 10212 10216 10218 10222 10228 10230 10236 10240 10242 10246 10248 10252 10254 10256 10257 10258 10260 10261 10262 10264 10266 10270 10272 10276 10278 10282 10288 10290 10296 10300 10302 10306 10312 10318 10320 10326 10330 10332 10338 10342 10348 10356 447348
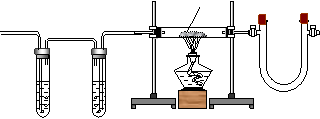
 CuO
CuO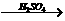 CuSO4
CuSO4