摘要:3.已知:H2(g)+F2+270 kJ.下列说法正确的是 ( ) A.2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量 B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ C.在相同条件下.1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 D.1 个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 [解析] A项中热化学方程式的化学计量数只表示物质的量,B项中气态HF变成液态HF要放出热量.故应大于270 kJ,C项中由高能量的反应物生成低能量的生成物才放出热量,D项中1 mol H2和1 mol F2反应生成2 mol HF放出的热量才是270 kJ. [答案] C
网址:http://m.1010jiajiao.com/timu3_id_88815[举报]
已知:
①H2(g)![]() 2H(g) ΔΗ1=+431.8 kJ·mol-1
2H(g) ΔΗ1=+431.8 kJ·mol-1
②![]() O2(g)
O2(g)![]() O(g) ΔΗ2=+244.3 kJ·mol-1
O(g) ΔΗ2=+244.3 kJ·mol-1
③2H(g)+O(g)![]() H2O(g) ΔΗ3=-917.9 kJ·mol-1
H2O(g) ΔΗ3=-917.9 kJ·mol-1
④H2O(g)![]() H2O(l) ΔΗ4=-44.0 kJ·mol-1
H2O(l) ΔΗ4=-44.0 kJ·mol-1
写出1 mol H2(g)与适量O2(g)生成H2O(l)反应的热化学方程式 。
查看习题详情和答案>>已知:H2(g)+F2(g)=2HF(g)△H=-539kJ/mol,若断裂1mol H-H键需吸收436kJ的能量,断裂1mol F-F键需吸收155kJ的能量,则断裂1mol H-F键需吸收的能量为( )
查看习题详情和答案>>
下列说法或表示方法正确的是( )
| A、由C(石墨)=C(金刚石)△H=+1.90 kJ?mol-1 可知金刚石比石墨稳定 | B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ | C、甲烷的标准燃烧热为△H=-890kJ?mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890 kJ?mol-1 | D、已知:H2(g)+F2(g)=2HF(g);△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
已知:H2(g)+F2(g)→2HF(g)+270kJ/mol,下列说法正确的是( )
| A、在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | B、1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ | C、该反应的逆反应是放热反应 | D、该反应过程的能量变化可用如图来表示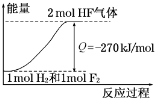 |