网址:http://m.1010jiajiao.com/timu3_id_86873[举报]
(14分)某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种的混合物,让同学们通过实验探究来确定。某同学探究过程如下:
(1) 提出假设:
假设1:黑色粉末是炭粉;
假设2:黑色粉末是氧化铜;
假设3:_________________________________________________________________。
(2) 设计实验方案:
他对实验做了如下设想和分析:取少量黑色粉末于烧杯中,并加入过量的稀硫酸。则实验中可能出现的现象与对应结论如下表,请你完成下表。
| 实验中可能出现的现象 | 结论 |
| ① | 假设1成立 |
| ② | 假设2成立 |
| ③ | 假设3成立 |
(4) 拓展:为了进一步探究炭粉和氧化铜的性质,他又利用这种混合物补充做了如下实验,将此黑色粉末隔绝空气加热(若炭完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请完成下列各题:
①烧杯中________(填“有”或“无”)不溶物;
②若静置后溶液呈无色,则该溶液中溶质是________(写化学式);
③若静置后溶液呈蓝色,该反应的化学方程式为:
________________________________________________________________________。 查看习题详情和答案>>
某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种的混合物,让同学们通过实验探究来确定。某同学探究过程如下:
(1)提出假设:
假设1:黑色粉末是炭粉;
假设2:_________________________________________________________________;
假设3:_________________________________________________________________。
(2)设计实验方案:
他对实验做了如下设想和分析:取少量黑色粉末于烧杯中,并加入过量的稀硫酸。则实验中可能出现的现象与对应结论如下表,请你完成下表。
|
实验中可能出现的现象 |
结论 |
|
① |
假设1成立 |
|
② |
假设2成立 |
|
③ |
假设3成立 |
(3)进行实验:通过实验及分析,确定该黑色物质为炭粉和氧化铜的混合物。
(4)拓展:为了进一步探究炭粉和氧化铜的性质,他又利用这种混合物补充做了如下实验,将此黑色粉末隔绝空气加热(若炭完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请完成下列各题:
①烧杯中________(填“有”或“无”)不溶物;
②若静置后溶液呈无色,则该溶液中溶质是________(写化学式);
③若静置后溶液呈蓝色,该反应的化学方程式为:
________________________________________________________________________。
查看习题详情和答案>>
(14分)某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种的混合物,让同学们通过实验探究来确定。某同学探究过程如下:
(1) 提出假设:
假设1:黑色粉末是炭粉;
假设2:黑色粉末是氧化铜;
假设3:_________________________________________________________________。
(2) 设计实验方案:
他对实验做了如下设想和分析:取少量黑色粉末于烧杯中,并加入过量的稀硫酸。则实验中可能出现的现象与对应结论如下表,请你完成下表。
|
实验中可能出现的现象 |
结论 |
|
① |
假设1成立 |
|
② |
假设2成立 |
|
③ |
假设3成立 |
(3) 进行实验:通过实验及分析,确定该黑色物质为炭粉和氧化铜的混合物。
(4) 拓展:为了进一步探究炭粉和氧化铜的性质,他又利用这种混合物补充做了如下实验,将此黑色粉末隔绝空气加热(若炭完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请完成下列各题:
①烧杯中________(填“有”或“无”)不溶物;
②若静置后溶液呈无色,则该溶液中溶质是________(写化学式);
③若静置后溶液呈蓝色,该反应的化学方程式为:
________________________________________________________________________。
查看习题详情和答案>>
某校进行化学实验考查时,教师给了同学一小包黑色粉末,这种黑色粉末可能是氧化铜、木炭粉或者是两者的混和物,让他们通过实验探究来确定.某同学的探究过程如下:
(1)[提出假设]
假设1:黑色粉末是木炭粉;
假设2:______________;
假设3:______________.
(2)[设计实验方案]他对实验做了如下设想和分析:
取少量粉末于烧杯中,并加入适量的稀硫酸.则实验中可能出现的现象与对应结论如下表.

(3)[进行实验]通过实验及分析,确定该黑色物质为木炭粉和氧化铜的混合物.
(4)[拓展]为了进一步探究木炭粉和氧化铜的性质,他又利用这种混合物补充做了如下实验:将此黑色粉末隔绝空气加热(若木炭粉完全反应),待冷却至室温后,取剩余固体于烧杯中,再加入适量稀硫酸,反应完全后,静置.
请你回答:
〈1〉烧杯中________(填“有”或“无”)不溶物;
〈2〉若静置后溶液呈无色,则该溶液中的溶质是________(写化学式);
〈3〉若静置后溶液呈蓝色,该反应的化学方程式为________.
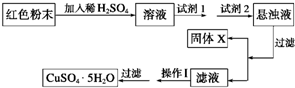 某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物.
某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物.己知:①Cu2O溶于稀硫酸生成Cu和CuSO4,②Cu2O在空气中加热生成CuO.
(1)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为
| 100(b-a) |
| a |
| 100(b-a) |
| a |
(2)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4?5H2O).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | 供选择试剂 | |
| Fe3+ | 1.9 | 3.7 | A.氯水,B.H2O2, C.NaOH,D.氨水, E.CuO,F.Cu2(OH)2CO3 |
| Fe2+ | 7.5 | 11 | |
| Cu2+ | 6.0 | 10 |
试回答:
①试剂1可以为
②固体X的化学式为
③操作Ⅰ为