网址:http://m.1010jiajiao.com/timu3_id_85652[举报]
铅蓄电池是典型的可充电电池,它的正负极极板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO![]()
![]() 2PbSO4+2H2O
2PbSO4+2H2O
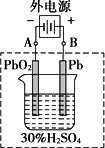
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时,正极的电极反应式是________;
电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g.
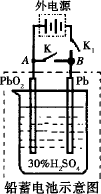
(2)在完全放电耗尽PbO2和Pb时,若按上图连接,电解一段时间后,则在A电极上生成________,B电极上生成________,此时铅蓄电池的正负极的极性将________.
Pb+PbO2+4H++2![]()
![]() 2PbSO4+2H2O,现有装置如下图,则下列说法正确的是
2PbSO4+2H2O,现有装置如下图,则下列说法正确的是
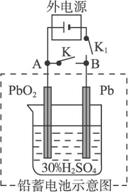
A.放电时负极反应是Pb-2e-====Pb2+,充电时阴极反应是PbSO4+2H2O-2e-====PbO2+4H+ +![]()
B.闭合K断开K1,电流的方向是从B到A
C.放电过程中,溶液的pH不断减小
D.放电时,线路上若有1 mol电子通过,则消耗硫酸也是1 mol
查看习题详情和答案>>铅蓄电池是典型的可充电电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO42— 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
放电时:正极的电极反应式是______________________________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
Pb+PbO2+4H++2SO42—
 2PbSO4+2H2O
2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
放电时:正极的电极反应式是______________________________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
|
铅蓄电池是典型的可充电电池,它的正负极隔板是惰性材料,电池总反应式为:
| |
| [ ] | |
A. |
放电时负极反应是:Pb-2e- |
B. |
闭合K断开K1,电流的流动方向是从B到A |
C. |
放电过程中,溶液的pH不断减小 |
D. |
放电时,线路上若有1 mol e-通过,则消耗硫酸也是1 mol |