网址:http://m.1010jiajiao.com/timu3_id_83945[举报]
 (2013?保定一模)某校化学兴趣小组设计了如下实验装置(图中部分夹持仪器已略去)来测 定某铁碳合金中铁的质量分数,并探究铁与浓硫酸的反应.请回答下列问题:
(2013?保定一模)某校化学兴趣小组设计了如下实验装置(图中部分夹持仪器已略去)来测 定某铁碳合金中铁的质量分数,并探究铁与浓硫酸的反应.请回答下列问题:(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现彖,其原 因是①
(2)点燃酒精灯,可观察到B中的现象是
(3)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg.则铢碳合金 中铁的质量分数为
| 3b |
| 11m |
| 3b |
| 11m |
(4)兴趣小组使用设计的如图实验装置,操作正确,且每一个反应均完全,仍然发现所测得的铁碳合金中铁的质量分数偏低,其主要原因是
(5)若反应一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:
2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑
然而,过氧化钠与其他非金属氧化物(如:NO、NO2等)的反应能否发生呢?为此,某校化学兴趣小组设计了以下实验进行探究:
步骤一:NO、NO2的制备
①本实验所用的NO由饱和硫酸亚铁溶液与浓硫酸和粉末状硝酸钾反应制备,在酸性环境中硝酸根离子被还原为NO,得到的NO的纯度约为98%;
反应的化学方程式为:
②NO2由硝酸铅受热分解得到:2Pb(NO3)2=2PbO+4NO2↑+O2↑使生成的气体通过
A.装有H2O的洗气瓶 B.置于冰水中的U形管(NO2沸点21℃)
C.装有浓硫酸的洗气瓶 D.装有Na2SO3溶液的洗气瓶
步骤二:操作(如图,b、c为弹簧夹)
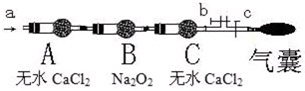
①先打开b关闭c,通入
A.空气 B.O2C.CO2 D.N2
②然后
现象:当通入NO时,B中靠近A侧浅黄色固体变成黄色,气囊未见鼓起;当通入NO2时,B中靠近A侧浅黄色固体变成白色,气囊也未见鼓起;
步骤三:产物检验
分别取出B中黄色固体或白色固体进行检验,得知两种固体均为盐.
结论:
请写出NO2与 Na2O2反应的化学方程式:

(1)往铁碳合金中加入浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
①常温下碳与浓硫酸不反应;②
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式
| ||
| ||
(3)B中的现象是:
(4)甲同学认为利用装置Ⅰ测得铁的质量分数偏大,请你写出可能的原因:
(5)乙同学认为用装置Ⅰ操作较繁杂,于是他设计了图示装置Ⅱ,若再使用其它仪器可测得如下数据:
①反应前后干燥管质量差a g ②反应前后装置和药品的总质量之差b g
③用排水法得H2的体积V L ④反应后过滤、洗涤、干燥得残渣质量c g
试选用上述数据,以简便和精确地测算铁的质量分数,其代数式为
| m-c |
| m |
| m-c |
| m |
(14分)
某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
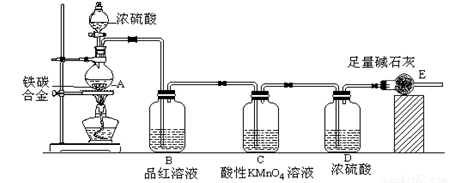
⑴ m克铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是
①常温下碳与浓硫酸不反应;② 。
⑵写出加热时A中碳与浓硫酸发生反应的化学方程式 。
⑶B中的现象是: ;C的作用是: 。
⑷待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为 (写表达式)。
⑸甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因: 。
⑹最后对所得测量结果进行评价,小组内有同学提出,本套装置在设计上存在多处缺陷而导致实验结果不准确,其中会导致铁质量分数测量值偏低是(任答一条即可) 。
查看习题详情和答案>>
某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数.
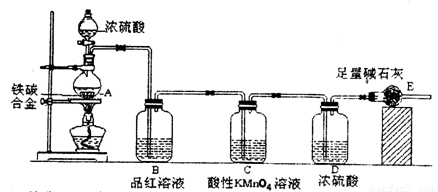
(1)m g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因
是:①常温下碳与浓硫酸不反应;②_____________。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式____________。
(3)B中的现象是:____________;C的作用是:_______________。
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。则铁碳合金中铁的质量分数为_____________。
(5)甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:___________。
(6)最后对所得测量结果进行评价,小组内有同学提出,本套装置在设计上存在多处缺陷而导致实验结果不准确,其中会导致铁质量分数测量值偏低的是(任答一条即可)
_____________。
查看习题详情和答案>>