摘要:化学用语 [方法指导] ① 习惯成自然.细节决定成败.要求学生养成良好的书写习惯.不漏.不忘.不添.不减. ② 要不断纠正从各次考试中发现的书写错误.要及时寻找错写原因.逐渐减少错误点. 知识网路 重点:考查对化学基本用语的掌握程度
网址:http://m.1010jiajiao.com/timu3_id_83225[举报]
离子反应是中学化学中重要的反应类型.回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.

(3)离子方程式是中学生应熟练掌握的化学用语,请写出下列反应的离子方程式:
向Ba(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,反应的离子方程式
在上述溶液中继续滴入NaHSO4溶液,此时离子方程式为
查看习题详情和答案>>
(1)在发生离子反应的反应物或生成物中,一定存在
③⑤
③⑤
.①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.

(3)离子方程式是中学生应熟练掌握的化学用语,请写出下列反应的离子方程式:
向Ba(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,反应的离子方程式
Ba2++SO42-+H++HCO3-═BaSO4+H2O+CO2↑
Ba2++SO42-+H++HCO3-═BaSO4+H2O+CO2↑
.在上述溶液中继续滴入NaHSO4溶液,此时离子方程式为
H++HCO3-═H2O+CO2↑
H++HCO3-═H2O+CO2↑
.如图是化学实验室中常用制备、干燥气体的部分仪器装置.某学校同学利用中学常用试剂及仪器设计下列实验.
(1)甲同学利用如图I装置制备并收集干燥的NO2气体,请完成下列问题:
①图I中仪器B的名称:
③B中发生反应的离子方程式为
④将收集满NO2的集气瓶浸入冰水中,烧瓶内气体颜色
(2)乙同学利用图Ⅰ装置制取氨气和氧气的混合气体,并且利用图Ⅱ装置验证氨的某些性质.A中加入浓氨水,B中加入过氧化钠固体,C中加入碱石灰,E内放置催化剂(铂石棉),按气流方向连接各仪器 a→b→c→h.请完成下列问题:
①实验中观察到E内有红棕色气体出现,证明氨气具有
②E中发生反应的化学方程式为
查看习题详情和答案>>
(1)甲同学利用如图I装置制备并收集干燥的NO2气体,请完成下列问题:

①图I中仪器B的名称:
圆底烧瓶
圆底烧瓶
;②收集NO2的方法向上排气法
向上排气法
;③B中发生反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑
3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑
.④将收集满NO2的集气瓶浸入冰水中,烧瓶内气体颜色
变浅
变浅
(填“变深”、“不变”或“变浅”),使用化学用语和必要的文字说明颜色变化的原因2NO2?N2O4△H<0,降低温度,平衡向放热方向即正反应方向移动,导致二氧化氮气体的浓度降低
2NO2?N2O4△H<0,降低温度,平衡向放热方向即正反应方向移动,导致二氧化氮气体的浓度降低
.(2)乙同学利用图Ⅰ装置制取氨气和氧气的混合气体,并且利用图Ⅱ装置验证氨的某些性质.A中加入浓氨水,B中加入过氧化钠固体,C中加入碱石灰,E内放置催化剂(铂石棉),按气流方向连接各仪器 a→b→c→h.请完成下列问题:
①实验中观察到E内有红棕色气体出现,证明氨气具有
还原
还原
性;②E中发生反应的化学方程式为
4NH3+5O2
4NO+6H2O;2NO+O2=2NO2
| ||
| △ |
4NH3+5O2
4NO+6H2O;2NO+O2=2NO2
.
| ||
| △ |
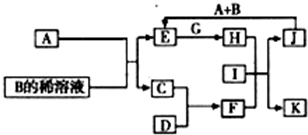 A-L为中学化学常见物质,其主要转化关系如图所示(其中产物水已略去).已知A为金属单质,C、D通常状况下为气体单质.B、F均为重要的化工产品,F为具有刺激性气味的气体,将一定量F通入B的稀溶液中可以得到两种盐K和L.G和I分别由相同的两种元素组成,通常状况下均为无色液体.
A-L为中学化学常见物质,其主要转化关系如图所示(其中产物水已略去).已知A为金属单质,C、D通常状况下为气体单质.B、F均为重要的化工产品,F为具有刺激性气味的气体,将一定量F通入B的稀溶液中可以得到两种盐K和L.G和I分别由相同的两种元素组成,通常状况下均为无色液体.(1)工业上冶炼金属A的方法称为
热还原法
热还原法
.(2)向E的溶液中加入氢氧化钠溶液的实验现象为
先生成白色沉淀,迅速变为灰绿色,最后变为红褐色
先生成白色沉淀,迅速变为灰绿色,最后变为红褐色
,反应的化学方程式为FeSO4+2NaOH=Na2SO4+Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3
FeSO4+2NaOH=Na2SO4+Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(3)写出E的酸性溶液与G反应转化为H的离子方程式
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.(4)相同条件下物质的量浓度相同的K、L溶液的pH大小关系为K
>
>
L(用“>”、“<”或“=”表示),其主要原因是(用化学用语说明)NH4++H2O?NH3?H2O+H+,HSO4-═H++SO42-
NH4++H2O?NH3?H2O+H+,HSO4-═H++SO42-
.某电镀铜厂有两种废水需要处理,一种废水中含有CN-离子,另一种废水中含有Cr2O72-离子.该厂拟定如图所示的废水处理流程.
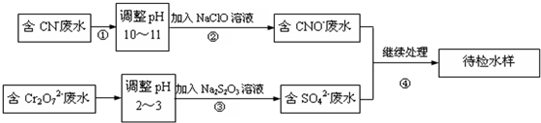
回答以下问题:
(1)上述处理废水的流程中主要使用的方法是
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因
(3)②中反应后无气体放出,该反应的离子方程式为
(4)③中反应时,每0.4molCr2O72-转移2.4mol的电子,该反应的离子方程式为
(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少.请你使用化学用语,结合必要的文字解释其原因
查看习题详情和答案>>

回答以下问题:
(1)上述处理废水的流程中主要使用的方法是
氧化还原法
氧化还原法
.(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因
ClO-+H2O HClO+OH-
HClO+OH-
 HClO+OH-
HClO+OH-ClO-+H2O HClO+OH-
HClO+OH-
. HClO+OH-
HClO+OH-(3)②中反应后无气体放出,该反应的离子方程式为
CN-+ClO-═CNO-+Cl-
CN-+ClO-═CNO-+Cl-
.(4)③中反应时,每0.4molCr2O72-转移2.4mol的电子,该反应的离子方程式为
3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O
3S2O32-+4Cr2O72-+26H+═6SO42-+8Cr3++13H2O
.(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少.请你使用化学用语,结合必要的文字解释其原因
待检水样中还有Cu2+,加碱发生Cu2++2OH-═Cu(OH)2↓,再加入Na2S溶液,CuS比Cu(OH)2更难溶,则发生Cu(OH)2(s)+S2-(aq)═CuS(s)+2OH-(aq)
待检水样中还有Cu2+,加碱发生Cu2++2OH-═Cu(OH)2↓,再加入Na2S溶液,CuS比Cu(OH)2更难溶,则发生Cu(OH)2(s)+S2-(aq)═CuS(s)+2OH-(aq)
.(2013?天津模拟)下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:

(1)④、⑤、⑦的原子半径由大到小的顺序为
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为
 .在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式
.在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性.

①写出D溶液与G反应的化学方程式
②写出检验A溶液中溶质的阴离子的方法:
③常温下,若电解1L 0.1mol/L A溶液,一段时间 后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为
④若图中各步反应均为完全转化,则混合物X中含有的物质有
查看习题详情和答案>>

(1)④、⑤、⑦的原子半径由大到小的顺序为
Na>Cl>F
Na>Cl>F
.(2)⑥和⑦的最高价含氧酸的酸性强弱为
HClO4
HClO4
>H2SO4
H2SO4
.(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为


H2O2+2Fe2++2H+=2Fe3++2H2O
H2O2+2Fe2++2H+=2Fe3++2H2O
.(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性.

①写出D溶液与G反应的化学方程式
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.②写出检验A溶液中溶质的阴离子的方法:
取少量A溶液滴加几滴(稀硝酸酸化的)硝酸银溶液有白色沉淀生成
取少量A溶液滴加几滴(稀硝酸酸化的)硝酸银溶液有白色沉淀生成
.③常温下,若电解1L 0.1mol/L A溶液,一段时间 后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为
0.01
0.01
mol.④若图中各步反应均为完全转化,则混合物X中含有的物质有
Al(OH)3、H2O、NaCl
Al(OH)3、H2O、NaCl
.