摘要:4.(2010·菏泽一中1月考题)下图表示各物质之间的转化关系.已知:常温下D.E.F.I.J为气体.且D.I是水煤气的主要成分,B是无色液体.M为红褐色固体.C的焰色反应为黄色.请回答下列问题: (1)基于反应①的化学工业称为 .写出该反应的化学方程式: . (2)写出K和E反应的离子方程式: . 写出F溶液和H反应的离子方程式: . (3)已知:由1 mol G分解得到的H.I.J三者的物质的量之比为1∶1∶1.则G的化学式为 . 解析:突破点1:D.I是水煤气的主要成分且D是电解的产物之一.判断D为H2.I为CO,突破点2:“LM .推断L是Fe(OH)2.M是Fe(OH)3,突破点3:B是无色液体.CO与B反应生成H2和J.可见J为CO2.B为H2O,结合其它信息推断A为NaCl.C为NaOH.H为FeO.E为Cl2.K为FeCl2.F为HCl. 答案:(1)氯碱工业 2NaCl+2H2OH2↑+Cl2↑+2NaOH (2)2Fe2++Cl2===2Fe3++2Cl- FeO+2H+===Fe2++H2O (3)FeC2O4
网址:http://m.1010jiajiao.com/timu3_id_81649[举报]
常温下D、E、F、I、J为气体,H、I、J都为氧化物,J为非极性分子;C的焰色反应为黄色;M为红褐色的固体,由G分解得到的H、I、J三者的物质的量相等.下图表示各物质之间的转化关系,

试回答下列问题:
(1)写出L的化学式
(2)基于反应①原理的化学工业称为
(3)反应②的现象是
(4)写出反应③的化学方程式
(5)K溶液中加入Na2O2溶液后有红褐色沉淀和黄色溶液生成,若转移3iVA的电子,得到沉淀的质量为
查看习题详情和答案>>

试回答下列问题:
(1)写出L的化学式
Fe(OH)2
Fe(OH)2
,J的结构式O=C=O
O=C=O
(2)基于反应①原理的化学工业称为
氯碱工业
氯碱工业
,写出反应①的离子方程式:2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
(3)反应②的现象是
白色固体变为灰绿色进一步变为红褐色.
白色固体变为灰绿色进一步变为红褐色.
(4)写出反应③的化学方程式
FeC2O4
FeO+CO↑+CO2↑
| ||
FeC2O4
FeO+CO↑+CO2↑
| ||
(5)K溶液中加入Na2O2溶液后有红褐色沉淀和黄色溶液生成,若转移3iVA的电子,得到沉淀的质量为
214
214
g.常温下D、E、F、I、J为气体,其中E 为有色气体;H、I、J都为氧化物,其中I、J的相对分子质量相差16;C的焰色反应为黄色;M为红褐色的固体,G为草酸亚铁,由G分解得到的H、I、J三者的物质的量相等.下图表示各物质之间的转化关系.
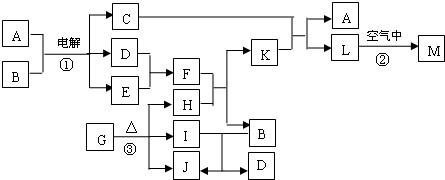
试回答下列问题:
(1)写出L的化学式 ,反应②的现象是 .
(2)足量的J与C反应生成N,下面是在实验室中模拟N的工业制法的实验装置:
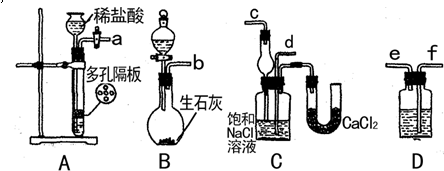
①装置的连接顺序是:(a)接 , 接 ;(b)接
②为了充分利用原料,A、B两装置中必须先发生反应的是 装置.
③C中用球形干燥管而不用直导管,其作用是 ,C中广口瓶内产生固体的总化学方程式为
(3)写出H与Al在高温下的反应方程式 .
(4)目前能量转化效率最高的是陶瓷电池.在750℃实验温度下,空气中的氧分子吸附于正极,氧原子会分别从涂层中“抢走”2个电子,变成氧离子后穿过陶瓷膜,与负极的燃气反应.若以D为上述陶瓷电池燃料气,则电池的负极反应方程式为 .
查看习题详情和答案>>

试回答下列问题:
(1)写出L的化学式
(2)足量的J与C反应生成N,下面是在实验室中模拟N的工业制法的实验装置:

①装置的连接顺序是:(a)接
②为了充分利用原料,A、B两装置中必须先发生反应的是
③C中用球形干燥管而不用直导管,其作用是
(3)写出H与Al在高温下的反应方程式
(4)目前能量转化效率最高的是陶瓷电池.在750℃实验温度下,空气中的氧分子吸附于正极,氧原子会分别从涂层中“抢走”2个电子,变成氧离子后穿过陶瓷膜,与负极的燃气反应.若以D为上述陶瓷电池燃料气,则电池的负极反应方程式为
下图表示各物质之间的转化关系,A、B、C、G为单质,其中A、G为气体,F为液体.②为工业生产中常见反应,E是一种具有漂白作用的盐,Y易潮解,M是一种两性化合物,L是一种白色胶状沉淀.
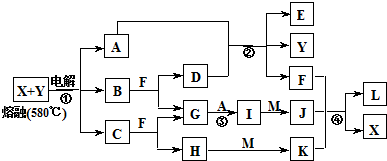
试回答下列有关问题:
(1)M的化学式 ,Y在实验室中的用途 (列举一例).
(2)X的熔点为801℃,实际工业冶炼中常常加入一定量的Y共熔,猜想工业上这样做的目的: .工业生产中,还常常利用电解X和F的混合物制取 .(填化学式)
(3)反应②的化学方程式是 .
(4)反应④的离子反应方程式是 .
(5)用化学方程式表示E在空气中失效的反应原理 .
查看习题详情和答案>>

试回答下列有关问题:
(1)M的化学式
(2)X的熔点为801℃,实际工业冶炼中常常加入一定量的Y共熔,猜想工业上这样做的目的:
(3)反应②的化学方程式是
(4)反应④的离子反应方程式是
(5)用化学方程式表示E在空气中失效的反应原理
下图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液。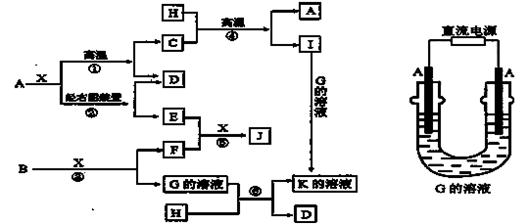
请按要求填空:
(1)写出B的电子式__________________________。
(2)写出生成E的电极反应式: ___________________________________。
反应⑤的现象是_______________________________。
(3)反应①的化学方程式是___________________ _______。
_______。
在实验室中引发反应④的操作是______________________。[来源:Z&xx&k.Com]
(4)反应⑥中若转移1 mol电子,则被还原的X是_____________mol。
下图表示各物质之间的转化关系,其中A、B、C、G为单质。②为工业生产中常见反应,E是一种具有漂白作用的盐,Y易潮解,M是一种两性化合物,L是一种白色沉淀。
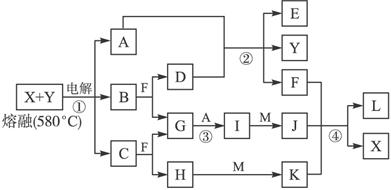
试完成下列有关问题:
(1)M的化学式___________,Y在实验室中的用途___________________________________(列举一例)。
(2)X的熔点为801 ℃,实际工业冶炼中常常加入一定量的Y共熔,猜想工业上这样做的目的:___________________________________。工业生产中,还常常利用电解X和F的混合物制取___________________________________________________。
(3)反应②的化学方程式是____________________________________________________。
(4)反应④的离子反应方程式是________________________________________________。
查看习题详情和答案>>