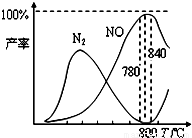
摘要:9.氨催化氧化是硝酸工业的基础.在某催化剂 作用下只发生主反应①和副反应②: 4NH3(g)+5O2(g) 4NO(g)+6H2O(g), ΔH=-905 kJ/mol ①. 4NH3(g)+3O2(g) 2N2(g)+6H2O(g), ΔH=-1 268 kJ/mol ②.反应①.②的产率与反应温度 的关系如图所示.下列说法正确的是 ( ) A.工业上进行氨催化氧化生成NO时.温度应控制在780-840℃ 之间 B.工业上采用物料比n(O2)/n(NH3)在1.7-2.0.主要是为了提高反应速率 C.在加压的条件下生产能力可提高5-6倍.是因为加压可提高转化率 D.氮气氧化为NO的热化学方程式为:N2(g)+O2,ΔH=+363 kJ/mol 解析:工业上进行氨催化氧化生成NO时.温度控制在780-840℃之间时NO的产率最高.故选项A说法正确,工业上采用物料比n(O2)/n(NH3)在1.7-2.0.目的是提高NH3的转化率,加压可提高生产能力.是因为提高了反应速率,由盖斯定律知N2(g)+O2,ΔH=+181.5 kJ/mol 答案:A
网址:http://m.1010jiajiao.com/timu3_id_80915[举报]
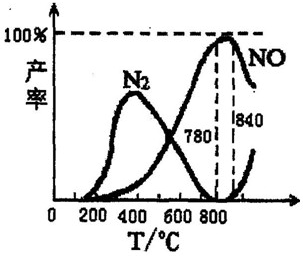 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图.
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图.①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ/mol
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ/mol
下列说法中不正确的是( )
| A、N2(g)+O2(g)?2NO(g);△H=+181.5 kJ/mol | B、加压有利于NH3生成NO,不利于NH3生成N2 | C、工业上氨催化氧化生成NO时,温度应控制在780~840℃之间 | D、工业上通常提高氧气的浓度,以提高NH3的转化率 |
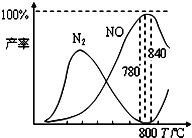 (2012?太原一模)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:
(2012?太原一模)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+905kJ
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)+1268kJ
有关物质产率与温度的关系如图.下列说法正确的是( )
查看习题详情和答案>>
 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图.4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1 ①4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1 ②下列说法中正确的是( )
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图.4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1 ①4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1 ②下列说法中正确的是( ) 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如右图。
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如右图。
4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
△H=-905 kJ·mol-1 ①
4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g)
2N2(g)+6H2O(g)
△H=-1268 kJ·mol-1 ②
下列说法中正确的是
A.工业上氨催化氧化生成 NO时,温度应控制在
780~840℃之间
B.工业上采用物料比n(O2)/n(NH??3)在1.7~2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
D.N2氧化为NO的热化学方程式为:N2(g)+O2(g)![]() 2NO(g) △H=-181.5 kJ·mol-1
2NO(g) △H=-181.5 kJ·mol-1