题目内容
 (2012?太原一模)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:
(2012?太原一模)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+905kJ
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)+1268kJ
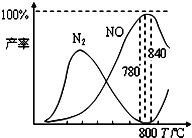
有关物质产率与温度的关系如图.下列说法正确的是( )
分析:A、从两个角度分析:一是比较NH3(g)+5O2(g) 4NO(g)+6H2O(g)反应前后气体的化学计量数关系,二是压强对平衡移动的影响;
4NO(g)+6H2O(g)反应前后气体的化学计量数关系,二是压强对平衡移动的影响;
B、从转化率的大小与温度的关系选择反应的适宜温度;
C、平衡常数的大小只与温度高低有关;
D、利用盖斯定律分析该类问题;
 4NO(g)+6H2O(g)反应前后气体的化学计量数关系,二是压强对平衡移动的影响;
4NO(g)+6H2O(g)反应前后气体的化学计量数关系,二是压强对平衡移动的影响;B、从转化率的大小与温度的关系选择反应的适宜温度;
C、平衡常数的大小只与温度高低有关;
D、利用盖斯定律分析该类问题;
解答:解:A、在NH3(g)+5O2(g) 4NO(g)+6H2O(g)反应中,反应物的化学计量数之和小于生成物的化学计量数之和,增大压强,平衡向逆反应方向移动,NO的转化率降低,故A错误;
4NO(g)+6H2O(g)反应中,反应物的化学计量数之和小于生成物的化学计量数之和,增大压强,平衡向逆反应方向移动,NO的转化率降低,故A错误;
B、从图象可以看在,反应温度在780~8400C之间,NO的产率最大,故B错误;
C、平衡常数只与温度有关,与反应物的浓度无关,故C正确;
D、根据盖斯定律进行计算,N2(g)+O2(g) 2NO(g)的反应热=
2NO(g)的反应热=
KJ/mol=-181.5KJ/mol,故D错误.
故选C.
 4NO(g)+6H2O(g)反应中,反应物的化学计量数之和小于生成物的化学计量数之和,增大压强,平衡向逆反应方向移动,NO的转化率降低,故A错误;
4NO(g)+6H2O(g)反应中,反应物的化学计量数之和小于生成物的化学计量数之和,增大压强,平衡向逆反应方向移动,NO的转化率降低,故A错误;B、从图象可以看在,反应温度在780~8400C之间,NO的产率最大,故B错误;
C、平衡常数只与温度有关,与反应物的浓度无关,故C正确;
D、根据盖斯定律进行计算,N2(g)+O2(g)
 2NO(g)的反应热=
2NO(g)的反应热=| 905-1268 |
| 2 |
故选C.
点评:本题考查化学平衡以及反应热的计算等问题,题目难度不大,注意对题中图象的分析以及盖斯定律的运用.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
 :和某聚碳酸酯工程塑料(
:和某聚碳酸酯工程塑料( )的原料之一.
)的原料之一.






 CuCl42-(aq)+4H2O(l)
CuCl42-(aq)+4H2O(l)