摘要:6.下列叙述正确的是( ) A.将5.85 g NaCl晶体溶于100 mL水中.制得0.1 mol·L-1 NaCl溶液 B.将1体积c mol·L-1硫酸溶液用水稀释为5体积.得到0.2c mol·L-1硫酸溶液 C.将25 g无水CuSO4溶于水制成100 mL溶液.其浓度为1 mol·L-1 D.将w g a%NaCl溶液蒸发掉w/2 g水.得到4a%NaCl溶液 解析:本题考查了一定物质的量浓度溶液的配制.溶液计算及计算能力的应用.较难题.A项中应将5.85 g NaCl晶体配成100 mL溶液.A不正确,C项中25 g无水硫酸铜的物质的量大于0.1 mol(注意:无水硫酸铜的摩尔质量为160 g/mol),D项中得到NaCl溶液的质量分数≤2a%. 答案:B
网址:http://m.1010jiajiao.com/timu3_id_79835[举报]
下列叙述正确的是
| A.将5.85 g NaCl晶体溶入100 mL水中,制得0.10 mol/L的NaCl溶液 |
| B.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol/L |
C.将w g a%的NaCl溶液蒸发掉 g水,可得到2a%的NaCl溶液( g水,可得到2a%的NaCl溶液( >2a%) >2a%) |
| D.将1体积c1mol/L的硫酸用水稀释为5体积,所得稀溶液的浓度为0.2c1mol/L |
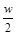 g水,可得到2a%的NaCl溶液(
g水,可得到2a%的NaCl溶液(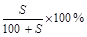 >2a%)
>2a%)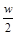 g水,可得到2a%的NaCl溶液(
g水,可得到2a%的NaCl溶液(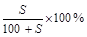 >2a%)
>2a%)