摘要:3.在纯水中.pH.[H+].[OH-]的关系肯定不正确的是 A.[H+] ﹥[OH-] B.[H+]﹥10-7 C.PH=6 D.PH﹥7
网址:http://m.1010jiajiao.com/timu3_id_79427[举报]
(1)25℃时,在酸性、碱性、中性溶液中,C(H+)?C(OH-)=
某温度下纯水中的C(H+)=2×10-7mol/L,则此时溶液中的C(OH-)=
(2)室温下取0.2mol?L-1HCl溶液与0.2mol?L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中水电离出的c(H+)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)=
(3)室温下如果取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度
(4)室温下,pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=7,则强碱与强酸的体积比是
查看习题详情和答案>>
10-14
10-14
.某温度下纯水中的C(H+)=2×10-7mol/L,则此时溶液中的C(OH-)=
2×10-7mol/L
2×10-7mol/L
mol/L;若温度不变,滴入稀盐酸,使c(H+)=5×10-4mol/L,则溶液中C(OH-)=8×10-11mol/L
8×10-11mol/L
mol/L,pH=8×10-11mol/L
8×10-11mol/L
.(2)室温下取0.2mol?L-1HCl溶液与0.2mol?L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中水电离出的c(H+)
>
>
0.2mol?L-1 HCl溶液中水电离出的c(H+);(填“>”、“<”、或“=”)②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)=
9.9×10-7
9.9×10-7
mol?L-1 c(H+)-c(MOH)=1.0×10-8
1.0×10-8
mol?L-1(3)室温下如果取0.2mol?L-1 MOH溶液与0.1mol?L-1 HCl溶液等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度
<
<
MCl的水解程度.(填“>”、“<”、或“=”),溶液中各离子浓度由大到小的顺序为c(Cl-)>c(M+)>c(H+)>c(OH-)
c(Cl-)>c(M+)>c(H+)>c(OH-)
.(4)室温下,pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=7,则强碱与强酸的体积比是
1:10
1:10
. Ⅰ(1)某温度下,纯水中的c (H+)=4.0×10-7 mol/L,则此温度下纯水中的
Ⅰ(1)某温度下,纯水中的c (H+)=4.0×10-7 mol/L,则此温度下纯水中的c(OH-)=
4.0×10-7
4.0×10-7
mol/L;若保持该温度不变,滴入稀NaOH溶液,使c(OH-)=5.0×10-6mol/L,则溶液的c(H+)=3.2×10-8
3.2×10-8
mol/L.(2)在25℃时,100ml 1.0mol/L的盐酸与等体积1.2mol/L的氢氧化钠溶液混合,混合后溶液的pH=
13
13
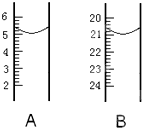
Ⅱ如图为中学常用定量仪器的部分结构(仪器被放大,单位mL),回答下列问题.
(1)写出两仪器名称:A
量筒
量筒
;B滴定管
滴定管
.(2)写出两仪器的读数:A
5.0mL
5.0mL
;B21.00mL
21.00mL
.(3)如果用B仪器取一定体积的液体,开始读数是平视刻度,结束读数是俯视刻度,则所取液体体积(填“偏大”、“偏小”或“不变”)
偏大
偏大
.(1)在25℃、101kPa下,1g乙烷燃烧生成CO2和液态水时放热QkJ.则表示乙烷燃烧热的热化学方程式为 .
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ?mol-1):
根据键能数据计算以下反应的反应热△H:CH4(g)+4F2(g)═CF4(g)+4HF(g)△H= .
(3)下列说法不正确的是(填序号) .
A.某温度下纯水中的c(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
C.相同温度下,0.1mol?L-1NH4Cl溶液中NH4+的浓度比0.1mol?L-1氨水中NH4+的浓度大
D.相同温度下,pH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.
查看习题详情和答案>>
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ?mol-1):
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
(3)下列说法不正确的是(填序号)
A.某温度下纯水中的c(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
C.相同温度下,0.1mol?L-1NH4Cl溶液中NH4+的浓度比0.1mol?L-1氨水中NH4+的浓度大
D.相同温度下,pH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.