摘要:16.如图.已知在△ABC中.∠ A=90°.请用圆规和直尺作⊙P.使圆心P在AC上.且与AB.BC两边都相切.(要求保留作图痕迹.不必写出作法和证明)
网址:http://m.1010jiajiao.com/timu3_id_7860[举报]
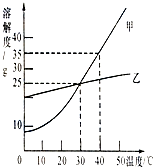 如图所示,填空:
如图所示,填空:(1)40℃时.甲物质溶解度为
(2)溶解度随温度变化影响比较大的物质是
(3)30℃时,向100g水中加入30g乙物质,充分溶解后,所得溶液是
(4)已知在水溶液中,乙醇(C2H5OH)不发生电离,碘化氢(HI)电离产生氢离子(H+)和碘离子(I-),氢氧化钠电离产生钠离子和氢氧根离子.请回答下列问题:
a.根据这三种溶液的组成推断,医用酒精(含乙醇75%的水溶液)显
b.写出上述物质之间发生中和反应的化学方程式
c.氢氧化钠溶液中存在的粒子有(用化学符号表示)
实验中学甲乙两组同学开展了下列研究性学习活动.
(一)、小组同学试验了氢氧化钠溶液、氯化钠溶液、稀硫酸、蒸馏水、乙醇的导电性试验.实验结果表明:乙醇不导电,蒸馏水几乎不导电,而氢氧化钠溶液、氯化钠溶液、稀硫酸却能导电.
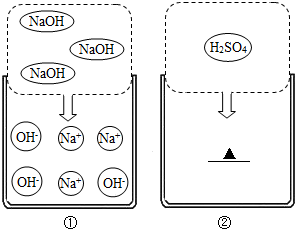
如图①是氢氧化钠在水溶液中的解离示意图.
(1)以氢氧化钠溶液为例,说明其导电的原因 ;
(2)试在如图②画出硫酸在水溶液中的离子(用离子符号表示)
于是他们联想到老师在电解水实验时,强调为增强水的导电性,需向蒸馏水加入了某些物质.因此他们找来了:氯化钠、硫酸、氢氧化钠、碳酸钙、胆矾.
(二)、(1)甲、乙两组同学向蒸馏水中分别加入某些物质,都形成无色透明溶液,小张同学推测:都没有加入碳酸钙、胆矾,其理由 .
(2)两组同学又测定溶液的pH,测定方法是 .甲组溶液的pH=13,则所加物质一定有 (写化学式). 乙组同学测得结果pH=7,则所加物质在水中解离出的阳离子(写离子符号) .
(3)甲组同学用如图装置进行电解水实验,检验试管b中产生的气体的操作方法是 .
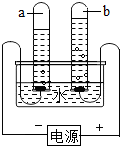
(4)试验完成后,甲组同学用试管取水槽内溶液适量,滴加硫酸铜溶液,产生蓝色沉淀,写出化学方程式 .
(三)、乙组同学也用上述相同的装置来电解某物质的水溶液,在试管b中产生黄绿色的气体,这是怎么回事呢?同学们一起向老师请教,知道了试管a是氢气,试管b中是氯气(Cl2).(至于什么原因,同学们将在今后学习中进一步研究)
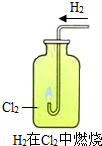
(1)在教师的指导下,查找资料,发现氢气在氯气中可以燃烧,化学方程式表示为H2+Cl2
2HCl.
试回答:①在试验氢气在氯气中燃烧之前,必须先检验氢气的 ;
②实验中可以观察到氢气燃烧,发出苍白色的火焰,同时瓶口有 ;
(2)比较氢气在空气中和在氯气中的燃烧,可以得出结论:
燃烧 要有氧气参加.(选填“一定”或“不一定”)
(3)现在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11:5:1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为 .
查看习题详情和答案>>
(一)、小组同学试验了氢氧化钠溶液、氯化钠溶液、稀硫酸、蒸馏水、乙醇的导电性试验.实验结果表明:乙醇不导电,蒸馏水几乎不导电,而氢氧化钠溶液、氯化钠溶液、稀硫酸却能导电.
如图①是氢氧化钠在水溶液中的解离示意图.
(1)以氢氧化钠溶液为例,说明其导电的原因
(2)试在如图②画出硫酸在水溶液中的离子(用离子符号表示)

于是他们联想到老师在电解水实验时,强调为增强水的导电性,需向蒸馏水加入了某些物质.因此他们找来了:氯化钠、硫酸、氢氧化钠、碳酸钙、胆矾.
(二)、(1)甲、乙两组同学向蒸馏水中分别加入某些物质,都形成无色透明溶液,小张同学推测:都没有加入碳酸钙、胆矾,其理由
(2)两组同学又测定溶液的pH,测定方法是
(3)甲组同学用如图装置进行电解水实验,检验试管b中产生的气体的操作方法是

(4)试验完成后,甲组同学用试管取水槽内溶液适量,滴加硫酸铜溶液,产生蓝色沉淀,写出化学方程式
(三)、乙组同学也用上述相同的装置来电解某物质的水溶液,在试管b中产生黄绿色的气体,这是怎么回事呢?同学们一起向老师请教,知道了试管a是氢气,试管b中是氯气(Cl2).(至于什么原因,同学们将在今后学习中进一步研究)

(1)在教师的指导下,查找资料,发现氢气在氯气中可以燃烧,化学方程式表示为H2+Cl2
| ||
试回答:①在试验氢气在氯气中燃烧之前,必须先检验氢气的
②实验中可以观察到氢气燃烧,发出苍白色的火焰,同时瓶口有
(2)比较氢气在空气中和在氯气中的燃烧,可以得出结论:
燃烧
(3)现在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11:5:1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为
某化工厂处理含铜废料,并生产氧化铜,生产流程如图:
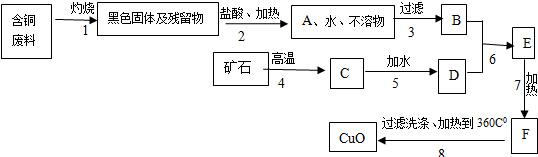
已知:
★生产流程中的矿石是种常见的建筑材料;
★过程1得到的残留物不溶于水和稀盐酸;
★过程6中恰好完全反应;
★Cu(OH)2在水中是胶状沉淀,很难过滤;
★CaCl2受热后很难分解,且溶解度随温度升高而增大;
★Cu(OH)2受热后极易分解成CuO和H2O;
(1)A、C处主要成份的化学式是: 、 .
(2)流程7处加热的主要目的是: .
(3)B、F处的混合物分别属: 、 (填写:溶液、乳浊液、悬浊液)
(4)完成生产流程1、7处的化学方程式: 、
(5)如果化工厂要制得铜,则应在B处加入过量的 (写化学式)及必要的作操.写出B处发生的主要化学反应方程式: .
查看习题详情和答案>>

已知:
★生产流程中的矿石是种常见的建筑材料;
★过程1得到的残留物不溶于水和稀盐酸;
★过程6中恰好完全反应;
★Cu(OH)2在水中是胶状沉淀,很难过滤;
★CaCl2受热后很难分解,且溶解度随温度升高而增大;
★Cu(OH)2受热后极易分解成CuO和H2O;
(1)A、C处主要成份的化学式是:
(2)流程7处加热的主要目的是:
(3)B、F处的混合物分别属:
(4)完成生产流程1、7处的化学方程式:
(5)如果化工厂要制得铜,则应在B处加入过量的
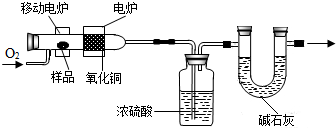 科学实验上测定有机物中碳元素和氢元素的含量,最常用的方法是燃烧分析法.即把已知量的样品置于氧气流中,用氧化铜作催化剂,在750℃左右,样品全部被氧化为二氧化碳和水.实验装置如图所示:
科学实验上测定有机物中碳元素和氢元素的含量,最常用的方法是燃烧分析法.即把已知量的样品置于氧气流中,用氧化铜作催化剂,在750℃左右,样品全部被氧化为二氧化碳和水.实验装置如图所示: 16、某探究小组的同学取等质量的A,B金属,分别投入溶质质量分数相同的足量的盐酸中,生成氢气的质量(m)与时间(t)的关系如图(已知A,B元素在生成物中的化合价相同,均为+2价)下列根据如图所示信息得到的结论中,正确的选项是( )
16、某探究小组的同学取等质量的A,B金属,分别投入溶质质量分数相同的足量的盐酸中,生成氢气的质量(m)与时间(t)的关系如图(已知A,B元素在生成物中的化合价相同,均为+2价)下列根据如图所示信息得到的结论中,正确的选项是( )