摘要:2. 过氧化钠能与水反应.某同学在学习了这一反应后提出了以下说法.你认为正确的是( ) A.Na2O2是氧化剂.H2O是还原剂 B.Na2O2既作氧化剂.又作还原剂 C.氧化剂和还原剂的质量比为1∶1 D.在2Na2O2+2H2O===4NaOH+O2↑的反应中.转移的电子数为4e- 解析:在Na2O2与H2O反应中.Na2O2中O为-1价.其中有一部分升高到0价.有一部分降低到-2价.H2O中元素化合价未变.1 mol Na2O2在反应中转移电子为1 mol. 答案:BC
网址:http://m.1010jiajiao.com/timu3_id_78518[举报]
过氧化钠能与水反应,某同学在学习了这一反应后提出了以下说法,你认为正确的是
[ ]
A.Na2O2是氧化剂,H2O是还原剂
B.Na2O2既作氧化剂,又作还原剂
C.氧化剂和还原剂的质量比为1∶1
D.在2Na2O2+2H2O===4NaOH+O2↑的反应中,转移的电子数为4e-
查看习题详情和答案>>
B.Na2O2既作氧化剂,又作还原剂
C.氧化剂和还原剂的质量比为1∶1
D.在2Na2O2+2H2O===4NaOH+O2↑的反应中,转移的电子数为4e-
某同学用如图所示装置制取纯净的氧气.试回答下列问题:

(1)乙中Na2O2可能发生的反应有(写化学方程式)
(2)丙中NaOH溶液的作用是
(3)若把原装置连接顺序改为:甲→丙→丁→乙→戊,则在装置戊中能否收集 到氧气?
查看习题详情和答案>>

(1)乙中Na2O2可能发生的反应有(写化学方程式)
2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
.(2)丙中NaOH溶液的作用是
除去过量的二氧化碳
除去过量的二氧化碳
,丁中浓H2SO4的作用是除去氧气中的水蒸气(干燥氧气)
除去氧气中的水蒸气(干燥氧气)
.(3)若把原装置连接顺序改为:甲→丙→丁→乙→戊,则在装置戊中能否收集 到氧气?
不能
不能
_ (填“能”或“不能”),原因是氢氧化钠溶液吸收了二氧化碳,浓硫酸吸收了水蒸气,没有物质与Na2O2反应产生氧气
氢氧化钠溶液吸收了二氧化碳,浓硫酸吸收了水蒸气,没有物质与Na2O2反应产生氧气
.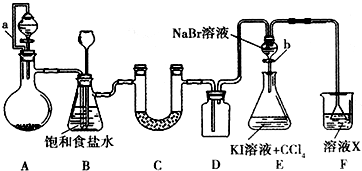 某同学设计如图所示的实验方案,请回答下列问题.
某同学设计如图所示的实验方案,请回答下列问题.(1)A装置的分液漏斗中盛装浓盐酸,烧瓶中固体为重铬酸钾(K2Cr2O7),还原产物是(CrCl3),写出A中反应的离子方程式
Cr2O72-+14H++6Cl-=2Cr3++3Cl2↑+7H2O
Cr2O72-+14H++6Cl-=2Cr3++3Cl2↑+7H2O
.(2)B装置有两个作用,分别是除去氯气中的氯化氢、
作安全瓶,防止实验过程中因导管堵塞而发生事故
作安全瓶,防止实验过程中因导管堵塞而发生事故
.拆去a导管的后果可能是浓盐酸不能顺利滴入烧瓶
浓盐酸不能顺利滴入烧瓶
.(3)U形管C中盛装的可以是
③
③
(填序号).①浓硫酸 ②碱石灰 ③无水CaCl2
(4)证明溴的非金属性比碘强的实验操作和现象是
实验完毕,打开活塞,使少量液体流入锥形瓶,关闭活塞,振荡锥形瓶,下层液体呈紫红色
实验完毕,打开活塞,使少量液体流入锥形瓶,关闭活塞,振荡锥形瓶,下层液体呈紫红色
;写出相应的离子方程式2I-+Br2=I2+2Br-
2I-+Br2=I2+2Br-
.(5)E装置中进行的实验存在明显不足,它是
没有排除氯气对溴单质与KI反应的干扰
没有排除氯气对溴单质与KI反应的干扰
,溶液X可以是①④⑥
①④⑥
(填序号).①氢氧化钠溶液②亚硫酸钠溶液③亚硫酸氢钠溶液④氯化亚铁溶液 ⑤硫氢化钠溶液 ⑥碳酸氢钠溶液.
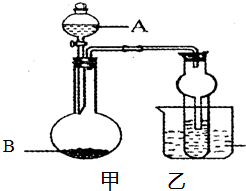 某同学设计如图所示的装置进行实验,请回答:
某同学设计如图所示的装置进行实验,请回答:(1)若试管内盛溴的四氯化碳溶液,液体A跟固体B(电石)在常温下反应,产生的气体可以使溴的四氯化碳溶液褪色,则A可能是
(2)若A为一种酸(HA)溶液,B为碳酸钠固体,试管内盛澄清的苯酚钠溶液,实验过程中观察到试管内溶液变浑浊,再加热烧杯中的水至70℃以上,观察到试管中的现象是
(3)本装置在不加热的条件下除制取乙炔外,还可以进行多种气体的制取和性质实验.请填写编号⑤栏目中的物质的名称或化学式(要求可制得的气体与示例的气体不同,而且设计要合理).
| 编号 | 液体A | 固体B | 可制得的气体 |
| ① | 浓氨水 | NaOH | NH3 |
| ② | 稀硫酸 | Zn | H2 |
| ③ | 稀盐酸 | CaC03 | C02 |
| ④ | 双氧水 | Mn02 | Q |
| ⑤ |
某同学创新设计制备氢氧化亚铁的实验方案:
(一)查阅资料
资料1:乙醇不与氢氧化钠或硫酸亚铁反应;乙醇与水互溶,氢氧化钠能溶于乙醇;硫酸亚铁在乙醇中的溶解度比在水中的溶解度小.氮气不能与铜反应.
资料2:几种含铁物质的颜色
| 化学式 | Fe | FeO | Fe2O3 | Fe3O4 | Fe(OH)2 | Fe(OH)3 |
| 颜色 | 银白色 | 黑色 | 红色 | 黑色 | 白色 | 红褐色 |
①取少量的新制硫酸亚铁晶体于大试管中,向其中加入5mL热蒸馏水,使之充分溶解,然后向其中慢慢加入10mL无水乙醇,这时会发现溶液中有小气泡逸出,静置,直到无小气泡冒出为止.
②另取一支试管,向其中加入半药匙固体氢氧化钠,然后向其中加入5mL无水乙醇,充分溶解后静置.
③用长胶头滴管吸取新配制的氢氧化钠的乙醇溶液,伸入硫酸亚铁溶液中,慢慢地挤压橡胶头,连续吸取几次,使之充分反应,静置片刻,这时在试管底会有大量的白色凝乳状溶胶沉降.
④小心地倒去上层溶液,再向试管中加入3mL无水乙醇洗涤,连续洗涤两三次,这时白色的凝乳状溶胶会变成白色固体,然后倒在滤纸上使乙醇充分挥发,便得到白色固体粉末.
(1)为避免硫酸亚铁在溶于水的过程中被氧化,通常可以向溶液中加入______.向硫酸亚铁溶液中慢慢加入无水乙醇时,产生气泡的原因是______.某同学制备无水乙醇的方法是向无水乙醇(含乙醇的质量分数为99.5%以上)中加入一定量的氯化钙,然后蒸馏得到无水乙醇,你认为此方法能否得到无水乙醇?______(填“能”或“否”).
(2)预测上述白色固体的成分可能是______,保持白色的主要原因是______.
(3)写出生成白色沉淀的化学方程式:______.
(三)探究产物成分
Ⅰ利用如图所示装置检验白色粉末的性质:
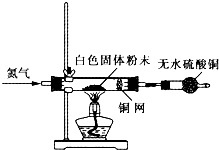
先通入氮气排尽装置内的空气后,继续通入氮气,然后加热硬质试管,观察到无水硫酸铜逐渐变成蓝色;硬质试管里的白色固体粉末逐渐变成黑色;铜网没有明显的颜色变化.当白色固体粉末全部变成黑色粉末时,停止加热,继续通入氮气至硬质试管冷却.
Ⅱ.待冷却后,取适量黑色粉末溶于少量的稀盐酸中,黑色粉末溶解,溶液呈浅绿色,不产生气泡.
Ⅲ.取Ⅱ中的溶液于试管中,滴加酸性高锰酸钾溶液,溶液的紫色褪去.
(4)实验1中,氮气的作用是______,铜网的作用是______.
(5)证明白色固体粉末中含有+2价铁的实验现象为______:写出符合要求的方程式:______.
属于分解反应的化学方程式:______;属于氧化还原反应的离子方程式:______
(6)某同学在上述实验的基础上,增加了一个实验确认白色固体中不含+3价铁,设计的实验可能是______. 查看习题详情和答案>>