摘要:2.下列二次根式中.与是同类二次根式的是( ) A. B. C. D.
网址:http://m.1010jiajiao.com/timu3_id_7736[举报]
根据下列装置图.回答有关问题:
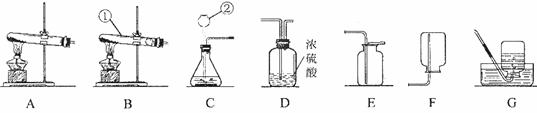
(1)写出装置中标号仪器的名称:① ;② 。
(2)实验室用高锰酸钾制取氧气,可选用的发生装置是 (填字母)。
(3)写出实验室制取二氧化碳的化学方程式 ,该反应
属于 反应(填基本反应类型)根据上图组装一套制取干燥CO2的装置 (用字母表示),验满的方法是 。
(4)某化学探究小组用盐酸与大理石反应研究影响反应剧烈程度的因素。实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10 g;所用盐酸的质量分数为9.125%、18.25%,每次实验盐酸的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1 g/cm3;大理石中杂质不与盐酸反应)。
①提出假设:盐酸与大理石反应的剧烈程度与所用盐酸的质量分数、大理石规格、反应温度有关。
②实验设计与实施:完成以下实验设计方案并实验。
| 实验 编号 | T/℃ | 大理石 规格 | 盐酸的 质量分数 | 完全反应 的时间/s | 实验目的 |
| a | 25 | 粗颗粒 | 18.25% | 160 | (I)实验a和b探究同体积下盐酸质量分数对该反应剧烈程度的影响。 (II)实验a和c探究温度对该反应剧烈程度的影响。 (Ⅲ)实验a和d探究大理石规格对该反应剧烈程度的影响。 |
| b | 210 | ||||
| c | 35 | 粗颗粒 | 18.25% | 60 | |
| d | 100 |
③实验结论: 。
查看习题详情和答案>>28、根据下列装置图.回答有关问题:

(1)写出装置中标号仪器的名称:①
(2)实验室用高锰酸钾制取氧气,可选用的发生装置是
(3)写出实验室制取二氧化碳的化学方程式
属于
(4)某化学探究小组用盐酸与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用盐酸的质量分数为9.125%、18.25%,每次实验盐酸的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应).
①提出假设:盐酸与大理石反应的剧烈程度与所用盐酸的质量分数、大理石规格、反应温度有关.
②实验设计与实施:完成以下实验设计方案并实验.
③实验结论:
查看习题详情和答案>>

(1)写出装置中标号仪器的名称:①
试管
;②长颈漏斗
.(2)实验室用高锰酸钾制取氧气,可选用的发生装置是
B
(填字母).(3)写出实验室制取二氧化碳的化学方程式
CaCO3+2HCl=CaCl2+CO2↑
,该反应属于
复分解
反应(填基本反应类型)根据上图组装一套制取干燥CO2的装置CDE
(用字母表示),验满的方法是将燃着的木条放在集气瓶口,木条熄灭说明已满
.(4)某化学探究小组用盐酸与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用盐酸的质量分数为9.125%、18.25%,每次实验盐酸的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应).
①提出假设:盐酸与大理石反应的剧烈程度与所用盐酸的质量分数、大理石规格、反应温度有关.
②实验设计与实施:完成以下实验设计方案并实验.
| 实验 编号 |
T/℃ | 大理石 规格 |
盐酸的 质量分数 |
完全反应 的时间/s |
实验目的 |
| a | 25 | 粗颗粒 | 18.25% | 160 | (I)实验a和b探究同体积下盐酸质量分数对该反应剧烈程度的影响. (II)实验a和c探究温度对该反应剧烈程度的影响. (Ⅲ)实验a和d探究大理石规格对该反应剧烈程度的影响. |
| b | 210 | ||||
| c | 35 | 粗颗粒 | 18.25% | 60 | |
| d | 100 |
在其他条件不变时,盐酸质量分数越大,反应越剧烈;温度越高,反应越剧烈;固体的颗粒越小,反应越剧烈.
.根据题意回答下列问题.

(1)写出图中有标号仪器的名称:a______、b______;
(2)用高锰酸钾制取氧气时,发生反应的符号表达式为______.该反应的反应类型是______
(3)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是______ (填序号),该反应的符号表达式为______.对此实验,让我们继续思考并研究几个问题:
问题①:催化剂二氧化锰(MnO2)的用量对反应速率有没有影响?
我的实验方案是:每次均用30mL10%的过氧化氢(H2O2)溶液,采用不同量二氧化锰(MnO2)粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 二氧化锰(MnO2)和粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间 | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 1 |
问题②:过氧化氢(H2O2)溶液的浓度对反应速率有没有影响?你的实验方案是:______
(4)实验室制取二氧化碳,可选用的发生装置为______,反应的符号表达式是______.收集二氧化碳气体可选用的收集装置为______,有时也可用碳酸钠来制备,请写出碳酸钠的化学式______.碳酸钠的相对分子质量为______.
(5)A装置中试管口略向下倾斜的原因是______.
(6)已知NO气体难溶于水,相同条件下密度略大于空气,极易与氧气反应.实验室收集NO的装置是______(填序号).
(7)采用C装置收集气体,如何判断收集满.______. 查看习题详情和答案>>
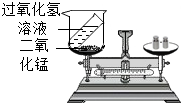 理解、掌握质量守恒定律是学好化学的基础.
理解、掌握质量守恒定律是学好化学的基础.(1)某同学按如图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡,请你用质量守恒定律解释其原因是
(2)由质量守恒定律可知,在化学反应前后,一定不变的是
①分子种类 ②原子种类 ③分子数目
④原子数目 ⑤物质质量 ⑥元素种类
(3)4.14玉树地震给当地人民造成巨大损失.为防止灾后发生疫情,必须对灾区进行消毒,其中的一种消毒剂是漂白粉,它的有效成分是次氯酸钙[Ca(ClO)2],次氯酸钙能与水和二氧化碳发生反应,请完成这个反应的化学方程式:Ca(ClO)2+CO2+H2O=CaCO3↓+2
(4)A、B、C三种物质各15g,它们化合时只生成30g新物质D.若增加10gA,则反应停止后,原反应物中只剩余B.根据上述条件推断下列说法中正确的是
A.该反应中,B是催化剂 B.第一次反应停止后,C剩余9g
C.第二次反应后,D的质量为50g D.反应中A和B的质量比是5:2
E.反应中A和C的质量比是5:2. 查看习题详情和答案>>
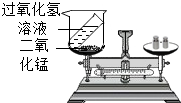 理解、掌握质量守恒定律是学好化学的基础.
理解、掌握质量守恒定律是学好化学的基础.