摘要: 近几年我国“神舟 系列飞船相继发射升空成功.这对增强我国的国防力量和国际地位都具有重要意义. 是发射航天飞船常用的高能燃料.将NH3和NaClO按一定物质的量比混合反应.生成肼.NaCl和水.该反应的化学方程式是 . (2)在火箭推进器中装有强还原剂肼和强氧化剂过氧化氢.当它们混合时.即产生大量气体.并放出大量热.已知:H2O,ΔH=+44 kJ·mol-1.12.8 g液态肼与足量过氧化氢反应生成氮气和水蒸气.放出256.65 kJ的热量. ①请写出液态肼与过氧化氢反应生成液态水的热化学方程式: . ②则16 g液态肼与液态双氧水反应生成液态水时放出的热量是 . ③此反应用于火箭推进.除释放大量热和快速产生大量气体外.还有一个很大的优点.你认为是 . (3)目前我国的液体火箭推进剂主要是结构简式为(CH3)2NNH2的偏二甲肼和N2O4.请写出该燃烧反应的化学方程式: . 第二节 燃烧热能源化学反应热的计算
网址:http://m.1010jiajiao.com/timu3_id_77340[举报]
近几年我国“神舟系列”飞船连续成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物A.已知该化合物A中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.回答下列问题:
(1)液态双氧水(过氧化氢)的电子式
 该分子是
该分子是
(2)A的结构式为
 该分子中的中心原子的杂化类型是
该分子中的中心原子的杂化类型是
(3)A能与硫酸反应生成B.B的结构与硫酸铵相似,则B的晶体内存在
查看习题详情和答案>>
(1)液态双氧水(过氧化氢)的电子式


极性
极性
分子(填“极性”或“非极性”)(2)A的结构式为


sp2
sp2
.若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,写出该反应的化学方程式N2H4+2H2O2═N2↑+4H2O
N2H4+2H2O2═N2↑+4H2O
.若该反应中有4mol N-H键断裂,则形成的π键有2
2
mol.(3)A能与硫酸反应生成B.B的结构与硫酸铵相似,则B的晶体内存在
abc
abc
(填标号) a.离子键 b.共价键 c.配位键 d.范德华力.近几年我国“神舟系列”飞船连续成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物A.已知该化合物A中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.回答下列问题:
(1)液态双氧水(过氧化氢)的电子式______ 该分子是______分子(填“极性”或“非极性”)
(2)A的结构式为______该分子中的中心原子的杂化类型是______.若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,写出该反应的化学方程式______.若该反应中有4mol N-H键断裂,则形成的π键有______mol.
(3)A能与硫酸反应生成B.B的结构与硫酸铵相似,则B的晶体内存在______(填标号) a.离子键 b.共价键 c.配位键 d.范德华力.
查看习题详情和答案>>
(1)液态双氧水(过氧化氢)的电子式______ 该分子是______分子(填“极性”或“非极性”)
(2)A的结构式为______该分子中的中心原子的杂化类型是______.若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,写出该反应的化学方程式______.若该反应中有4mol N-H键断裂,则形成的π键有______mol.
(3)A能与硫酸反应生成B.B的结构与硫酸铵相似,则B的晶体内存在______(填标号) a.离子键 b.共价键 c.配位键 d.范德华力.
近几年我国“神舟系列”飞船连续成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物A.已知该化合物A中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.回答下列问题:
(1)液态双氧水(过氧化氢)的电子式 该分子是 分子(填“极性”或“非极性”)
(2)A的结构式为 该分子中的中心原子的杂化类型是 .若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,写出该反应的化学方程式 .若该反应中有4mol N-H键断裂,则形成的π键有 mol.
(3)A能与硫酸反应生成B.B的结构与硫酸铵相似,则B的晶体内存在 (填标号) a.离子键 b.共价键 c.配位键 d.范德华力. 查看习题详情和答案>>
(1)液态双氧水(过氧化氢)的电子式 该分子是 分子(填“极性”或“非极性”)
(2)A的结构式为 该分子中的中心原子的杂化类型是 .若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的物质,写出该反应的化学方程式 .若该反应中有4mol N-H键断裂,则形成的π键有 mol.
(3)A能与硫酸反应生成B.B的结构与硫酸铵相似,则B的晶体内存在 (填标号) a.离子键 b.共价键 c.配位键 d.范德华力. 查看习题详情和答案>>
近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成的,此外,各种机动车排放的尾气也是形成酸雨的重要原因.
【提出问题】通过实验证明煤中含有碳元素和硫元素.
【查阅资料】
(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色)请完成该反应的化学方程式
SO2+ KMnO4+ H2O= K2SO4+ MnSO4+ H2SO4
根据上述资料,甲、乙、丙三位同学分别设计实验方案进行探究.
【实验探究】
甲同学:
“实验操作”:甲同学进行了如图1所示A、B两步实验:
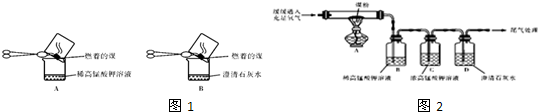
【实验现象】:A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊.
【得出结论】:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.
(2)乙同学认为甲同学的实验方案不合理,其理由是: .
丙同学:
【实验操作】:丙同学进行了如图2所示实验(部分装置在图中略去):
【探究与结论】
(3)上图C装置的作用是 .
(4)要证明煤中含有碳元素和硫元素的现象 .
查看习题详情和答案>>
【提出问题】通过实验证明煤中含有碳元素和硫元素.
【查阅资料】
(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色)请完成该反应的化学方程式
根据上述资料,甲、乙、丙三位同学分别设计实验方案进行探究.
【实验探究】
甲同学:
“实验操作”:甲同学进行了如图1所示A、B两步实验:

【实验现象】:A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊.
【得出结论】:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.
(2)乙同学认为甲同学的实验方案不合理,其理由是:
丙同学:
【实验操作】:丙同学进行了如图2所示实验(部分装置在图中略去):
【探究与结论】
(3)上图C装置的作用是
(4)要证明煤中含有碳元素和硫元素的现象
近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成的,此外,各种机动车排放的尾气也是形成酸雨的重要原因。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】
(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色)请完成该反应的化学方程式
SO2 + KMnO4 + H2O= K2SO4 + MnSO4 + H2SO4
根据上述资料,甲、乙、丙三位同学分别设计实验方案进行探究。
【实验探究】
甲同学:
“实验操作”:甲同学进行了如下图所示A、B两步实验:

“实验现象”: A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(2)乙同学认为甲同学的实验方案不合理,其理由是: 。
丙同学:
“实验操作”:丙同学进行了如下图所示实验(部分装置在图中略去):
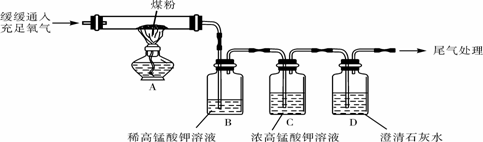
【探究与结论】
(3)上图C装置的作用是 。
(4)要证明煤中含有碳元素和硫元素的现象 。
查看习题详情和答案>>